
Wetenschap
Hoeveel halfgevulde orbitalen zitten er in een chlooratoom?
Hier leest u hoe u het aantal halfgevulde orbitalen in een chlooratoom kunt bepalen:
1. Elektronenconfiguratie:
* Chloor (CL) heeft een atoomnummer van 17, wat betekent dat het 17 elektronen heeft.
* De elektronenconfiguratie is:1S² 2S² 2P⁶ 3S² 3P⁵
2. Het identificeren van halfgevulde orbitalen:
* 3P Subblevel: Het 3P -sub -niveau heeft 3 orbitalen (3px, 3py, 3pz). Elk orbitaal kan maximaal 2 elektronen bevatten.
* Het 3P -subbleiveau heeft 5 elektronen. Dit betekent dat één orbitaal volledig is gevuld (2 elektronen), en de andere twee orbitalen zijn half gevuld (elk 1 elektron).
3. Antwoord:
Daarom zijn er twee halfgevulde orbitalen in een chlooratoom.
 Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen
Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen Stel dat u een suikeroplossing hebt en deze laat verdampen, waardoor kristallen achterblijven. Zijn deze mineralen?
Stel dat u een suikeroplossing hebt en deze laat verdampen, waardoor kristallen achterblijven. Zijn deze mineralen?  Heeft geen definitieve vorm vaste vloeistof of gas?
Heeft geen definitieve vorm vaste vloeistof of gas?  Worden elektronen gelijk gedeeld in CH4?
Worden elektronen gelijk gedeeld in CH4?  Hoe verandert water in een vaste stof?
Hoe verandert water in een vaste stof?
 Video:Levensonderhoud op een zandbank
Video:Levensonderhoud op een zandbank Het focussen op de aandacht op geselecteerde aspecten van de omgeving en het uitblazen van anderen is dat?
Het focussen op de aandacht op geselecteerde aspecten van de omgeving en het uitblazen van anderen is dat?  De bouwhausse in Florida bedreigt een lagune die rijk is aan wilde dieren
De bouwhausse in Florida bedreigt een lagune die rijk is aan wilde dieren Nieuwe studie van aardkorst toont wereldwijde groeispurt van drie miljard jaar geleden
Nieuwe studie van aardkorst toont wereldwijde groeispurt van drie miljard jaar geleden Waarom we de bedreigde status van de Komodovaraan opnieuw moeten beoordelen
Waarom we de bedreigde status van de Komodovaraan opnieuw moeten beoordelen
Hoofdlijnen
- Welke van de volgende paren protisten en hun kenmerken is niet overeengekomen?
- Onderzoek toont aan dat plantengroeiregulatoren gunstig kunnen zijn voor de vestiging van uien, productie
- Hoe cellen omgaan met gebroken chromosomen
- Politicoloog beschrijft de opkomst van negatieve partijdigheid en hoe dit kiezers drijft
- Waar gebruiken organismen lipiden voor?
- Wat is een celstructuur waarin functies worden uitgevoerd om het overleven te waarborgen?
- Wat wordt bedoeld met primitieve translationele vector?
- Wat is wetenschappelijk tijdschrift?
- Wat bedoel je met terminologie in termen van plantkunde?
- Onderzoekers ontdekken methode om kankerverwekkende formaldehydeafgifte uit hout in huis te beheersen

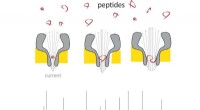
- Nanoporiën maken draagbare massaspectrometer voor peptiden werkelijkheid
- Bollen kunnen beton slanker maken, groener

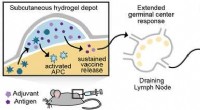
- Injecteerbare hydrogel kan ooit leiden tot effectievere vaccins
- Het water en het zweet opzuigen - een nieuw superdroogmiddel
 Circulatie van water in het diepe binnenste van de aarde
Circulatie van water in het diepe binnenste van de aarde 5 Onderdelen van een goed ontworpen wetenschappelijk experiment
5 Onderdelen van een goed ontworpen wetenschappelijk experiment MagicMark:een markeringsmenu met 2D-richting en 3D-diepte-informatie
MagicMark:een markeringsmenu met 2D-richting en 3D-diepte-informatie Analyseren waarom Wikipedia vaak verhalen over vrouwen in de geschiedenis over het hoofd ziet
Analyseren waarom Wikipedia vaak verhalen over vrouwen in de geschiedenis over het hoofd ziet  Binnen in het grootste aquarium van de VS:Georgia Aquarium
Binnen in het grootste aquarium van de VS:Georgia Aquarium  Hoe korrels van verschillende grootte worden beïnvloed door winderosie?
Hoe korrels van verschillende grootte worden beïnvloed door winderosie?  Waar zijn Amerikanen het meest bang voor? Onderzoekers publiceren 4e jaarlijkse Survey of American Fears
Waar zijn Amerikanen het meest bang voor? Onderzoekers publiceren 4e jaarlijkse Survey of American Fears Welke soorten mineralen eindigen als sedimenten?
Welke soorten mineralen eindigen als sedimenten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

