
Wetenschap
Welk type reactie vindt plaats wanneer een metaal corrosie ondergaat?
Hier is een uitsplitsing:
* oxidatie: De metaalatomen verliezen elektronen en worden positief geladen ionen. Dit proces wordt oxidatie genoemd.
* reductie: De elektronen verloren door de metaalatomen worden verkregen door een andere stof, meestal zuurstof of water. Dit proces wordt reductie genoemd.
Voorbeeld:roesten van ijzer
IJzer (Fe) reageert met zuurstof (O2) en water (H2O) om ijzeroxide (Fe2O3) te vormen, beter bekend als roest.
* oxidatie: Fe → fe²⁺ + 2e⁻
* reductie: O2 + 4E⁻ + 2H2O → 4OH⁻
De algemene reactie is:
4FE + 3O2 + 6H2O → 2Fe2O3 · 3H2O (roest)
Key Takeaways:
* Corrosie omvat de overdracht van elektronen.
* Oxidatie is het verlies van elektronen.
* Reductie is de winst van elektronen.
* Corrosie is een veel voorkomend en vaak destructief proces dat een breed scala aan materialen kan beïnvloeden.
 Tyfoon Phanfone verpest Kerstmis voor duizenden Filippino's
Tyfoon Phanfone verpest Kerstmis voor duizenden Filippino's Indonesië alert op nieuwe uitbarstingen bij afgelegen vulkaan
Indonesië alert op nieuwe uitbarstingen bij afgelegen vulkaan  Opwarming van de aarde treft zeedieren het hardst
Opwarming van de aarde treft zeedieren het hardst Nieuw model vereenvoudigt orbitale radar-afwegingsstudies voor milieumonitoring
Nieuw model vereenvoudigt orbitale radar-afwegingsstudies voor milieumonitoring Alles op tafel:onderzoekers pleiten voor een uitgebreidere beoordeling van het wereldwijde voedselsysteem
Alles op tafel:onderzoekers pleiten voor een uitgebreidere beoordeling van het wereldwijde voedselsysteem
Hoofdlijnen
- Studie vindt minder vogeldiversiteit in stadsbossen
- Wat zijn de vele kleinere moleculen die DNA vormen?
- Wat is een microscopisch cellen dier?
- Wat is de term voor eiwitten die materialen van de ene plaats naar de andere in het lichaam dragen?
- Onderzoekers ontdekken de sleutel tot het moleculaire mysterie van hoe planten reageren op veranderende omstandigheden
- Ideeën voor wetenschapsbeurzen Projecten met honden
- Waar komen Australische katten vandaan?
- Forest Service weegt wijzigingen in bescherming voor saliehoen af
- Hoe maak je een dierencel uit Candy
- Silicium met een tweedimensionale structuur
- Nieuwe STM-techniek wijst weg naar nieuwe en zuiverdere geneesmiddelen

- De meest complete studie van batterijstoringen ziet het licht
- Een snellere en betrouwbaardere methode om olijfolie te categoriseren is gevalideerd

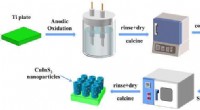
- CuInS2/TiO2-fotoanodecomposieten presteren goed in fotogeïnduceerde kathodische bescherming
 Is rivierwater een elementverbinding of mengsel?
Is rivierwater een elementverbinding of mengsel?  Op grafeen gebaseerde geheugenweerstanden zijn veelbelovend voor op de hersenen gebaseerd computergebruik
Op grafeen gebaseerde geheugenweerstanden zijn veelbelovend voor op de hersenen gebaseerd computergebruik Het blussen van de water- en energiecrises van de wereld, een kleine druppel per keer
Het blussen van de water- en energiecrises van de wereld, een kleine druppel per keer Hoe scheid je ammoniak van waterstof?
Hoe scheid je ammoniak van waterstof?  Waar veranderen warmte en druk aan van leisteen?
Waar veranderen warmte en druk aan van leisteen?  Hoe de douane werkt
Hoe de douane werkt  Hoe worden de planeten in hun baan gehouden?
Hoe worden de planeten in hun baan gehouden?  Waarom de wetenschap de geesteswetenschappen nodig heeft om klimaatverandering op te lossen
Waarom de wetenschap de geesteswetenschappen nodig heeft om klimaatverandering op te lossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

