
Wetenschap
Wat gebeurt er in de reactie tussen natriumhydroxide en magnesiumsulfaat?
1. Reactanten:
* Natriumhydroxide (NaOH) is een sterke basis.
* Magnesiumsulfaat (mgso₄) is een oplosbaar zout.
2. Producten:
* magnesiumhydroxide (mg (oh) ₂) wordt gevormd als een wit, gelatineus neerslag. Het is onoplosbaar in water.
* Natriumsulfaat (Na₂so₄) blijft opgelost in oplossing. Het is oplosbaar in water.
3. Evenwichtige chemische vergelijking:
2naOH (aq) + mgso₄ (aq) → mg (oh) ₂ (s) + na₂so₄ (aq)
4. Verklaring:
In deze reactie, de natrium (NA⁺) ionen van NaOH en de magnesium (mg²⁺) ionen van MGSO₄ -schakelpartners. De hydroxide (OH⁻) ionen van NaOH combineren met de magnesiumionen om magnesiumhydroxide te vormen, dat onoplosbaar is en uit oplossing neerslaat. De resterende natriumionen en sulfaationen blijven opgelost in de oplossing als natriumsulfaat.
5. Observaties:
* U zult de vorming waarnemen van een wit, bewolkt neerslag (magnesiumhydroxide) in de oplossing.
* De reactie is exotherme, wat betekent dat het warmte vrijgeeft en de oplossing zal enigszins warm aanvoelen.
6. Toepassingen:
Deze reactie wordt in verschillende toepassingen gebruikt, waaronder:
* Waterbehandeling: Magnesiumhydroxide wordt gebruikt als flocculant om onzuiverheden uit water te verwijderen.
* Productie van magnesiumverbindingen: Het neerslag kan worden gefilterd en verder worden verwerkt om magnesiumhydroxide te verkrijgen, dat in verschillende industrieën wordt gebruikt.
Laat het me weten als je nog andere vragen hebt!
 Van welk subatomair deeltje is een waterstofion gemaakt?
Van welk subatomair deeltje is een waterstofion gemaakt?  Onderzoekers dagen de grenzen van het moleculaire geheugen uit en openen de deur voor de ontwikkeling van moleculaire chips
Onderzoekers dagen de grenzen van het moleculaire geheugen uit en openen de deur voor de ontwikkeling van moleculaire chips  Egg in Bottle Science Projects
Egg in Bottle Science Projects  Wat zijn de subatomaire artikelen die kunnen veranderen tijdens een kernreactie?
Wat zijn de subatomaire artikelen die kunnen veranderen tijdens een kernreactie?  Waarom is radium een goede dirigent?
Waarom is radium een goede dirigent?
 Onderzoekers observeren een positieve trend in het wereldwijde herstel van ozon
Onderzoekers observeren een positieve trend in het wereldwijde herstel van ozon Is de Maya-beschaving geëindigd vanwege de klimaatverandering?
Is de Maya-beschaving geëindigd vanwege de klimaatverandering?  Kunnen teken eieren op mensen leggen?
Kunnen teken eieren op mensen leggen?  Arctische afbraak:wat klimaatverandering in het hoge noorden betekent voor de rest van ons
Arctische afbraak:wat klimaatverandering in het hoge noorden betekent voor de rest van ons Onderzoekers bestuderen bosbranden in Alaska in de afgelopen 450 jaar
Onderzoekers bestuderen bosbranden in Alaska in de afgelopen 450 jaar
Hoofdlijnen
- Als u een huidcel zou onderzoeken tijdens een complete cyclus, welke fase zou nooit waarnemen?
- Indringende vraag:Waarom worden albino's altijd als schurken neergezet?
- Wat kan er gebeuren voor een beperkte genenstroom?
- Hoe een 'dirigent' betekenis geeft aan chaos in vroege muizenembryo's
- Hoeveel moleculen ATP worden geproduceerd in het anaërobe metabolisme?
- Heeft de pH van water invloed op groeireparaten?
- Waar staat de kruising in mRNA voor?
- Waarom is replicatie belangrijk in de wetenschap?
- Waarom produceren gymnospermen en angiospermen pollenzaden?
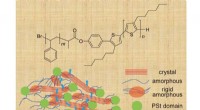
- Elektrische verbetering:ingenieurs versnellen elektronen in halfgeleiders
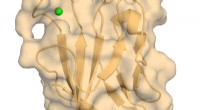
- Onderzoekers beeld atomaire structuur van belangrijke immuunregulator af
- Massaspectrometriebeeldvorming maakt ingrediënten, additieven en contaminanten van voedsel zichtbaar

- Onderzoekers produceren goedkope handdesinfecterende middelen uit afval

- Waterstof als traphulp

 Waarom worden alkalimetalen niet vrij in de natuur aangetroffen?
Waarom worden alkalimetalen niet vrij in de natuur aangetroffen?  Uit onderzoek blijkt hoe gewervelde dieren de Noordzeebodem vormgeven
Uit onderzoek blijkt hoe gewervelde dieren de Noordzeebodem vormgeven  Wat zijn de fysieke eigenschappen van de zon?
Wat zijn de fysieke eigenschappen van de zon?  Volgens onderzoek zorgt het bezoeken van witte delen van de stad ervoor dat sommige zwarte kinderen zich minder veilig voelen
Volgens onderzoek zorgt het bezoeken van witte delen van de stad ervoor dat sommige zwarte kinderen zich minder veilig voelen  Interactieve kaart laat zien hoe de Britse eilanden werden beïnvloed door de laatste glaciale cyclus 22, 000 jaar geleden
Interactieve kaart laat zien hoe de Britse eilanden werden beïnvloed door de laatste glaciale cyclus 22, 000 jaar geleden Phases of the Moon Activiteiten voor kinderen
Phases of the Moon Activiteiten voor kinderen  Landsat-erfenis:NASA–USGS-programma dat de aarde observeert vanuit de ruimte wordt 50
Landsat-erfenis:NASA–USGS-programma dat de aarde observeert vanuit de ruimte wordt 50 Klaar om te raketten
Klaar om te raketten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

