
Wetenschap
Waarom wordt zink niet geëxtraheerd uit oxide door reductie met behulp van koolmonoxide?
1. Zink's volatiliteit:
* Zink heeft een relatief laag kookpunt (907 ° C).
* Als u zinkoxide verwarmt met koolmonoxide tot temperaturen hoog genoeg om het te verminderen tot zinkmetaal, verdampt het zink. Dit maakt het moeilijk om het zink te verzamelen en te condenseren.
2. De beperkingen van koolmonoxide:
* Hoewel koolmonoxide een goed reductiemiddel is, is het niet sterk genoeg om zinkoxide effectief te verminderen bij temperaturen onder het kookpunt van zink.
3. Alternatieve methoden:
* elektrolyse: De meest voorkomende methode voor het extraheren van zink uit zijn oxide is door elektrolyse. Dit proces gebruikt een elektrische stroom om zinkionen te verminderen in een elektrolytoplossing, waardoor gesmolten zink wordt geproduceerd.
* carbothermische reductie (met cola): Deze methode omvat het verwarmen van zinkoxide met cola (een vorm van koolstof) tot een hoge temperatuur. De reactie produceert zinkdamp, die vervolgens wordt gecondenseerd en verzameld. Deze methode wordt vaak gebruikt in combinatie met elektrolyse.
Samenvattend:
Het lage kookpunt van zink maakt het moeilijk om het uit zijn oxide te extraheren met behulp van koolmonoxide. Elektrolyse en carbothermische reductie bieden effectievere en praktische methoden voor zinkextractie.
 Hoeveel soorten organische verbindingen zijn er?
Hoeveel soorten organische verbindingen zijn er?  Hoeveel ringen zijn er in de atoomstructuur van Cobalts?
Hoeveel ringen zijn er in de atoomstructuur van Cobalts?  Wat is de chemische formule van Mannose?
Wat is de chemische formule van Mannose?  Nieuwe kooldioxide-adsorberende kristallen voor biomedische materialen die afhankelijk zijn van vormgeheugeneffect
Nieuwe kooldioxide-adsorberende kristallen voor biomedische materialen die afhankelijk zijn van vormgeheugeneffect Welk element zit in de boorfamilie en de overvloedige metaalkorst?
Welk element zit in de boorfamilie en de overvloedige metaalkorst?
Hoofdlijnen
- Dodelijke vogelgriep keert eerder terug naar Midwest dan verwacht
- Zachte apparaten, aangedreven door gestresste algen, gloeien in het donker wanneer ze worden geplet of uitgerekt
- Producten geproduceerd door Anaerobe ademhaling
- Weten waar honden graag naar kijken, kan dierenartsen helpen hun gezichtsvermogen te beoordelen
- Als een organisme vijf paar chromosomen heeft, hoeveel verschillende gameten zou het dan kunnen produceren zonder over te steken?
- Wat zijn de doelcellen van erytropoëtine?
- Een beter nest ontwerpen om bedreigde schildpadden te helpen
- Een online ontmoeting met je hond? Studie test het vermogen van honden om acties te imiteren die worden waargenomen op videoprojecties
- Hoe reproduceren algen zich?
- Ademtests kunnen COVID-19 opsporen
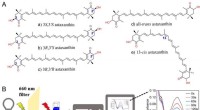
- Evaluatie van de antioxidantactiviteit van astaxanthine-isomeren tegen singletzuurstof
- Onderzoekers creëren nieuw glaskeramisch materiaal van industriële verontreinigingen

- Bacteriën kunnen een toekomstige bron van elektriciteit zijn
- Een nieuwe manier om kleuremissies van transparante films te moduleren

 Unievriendelijke staten genieten van een hogere economische groei, individuele inkomsten
Unievriendelijke staten genieten van een hogere economische groei, individuele inkomsten Kwantummechanische moleculen gespot in supergeleidende apparaten
Kwantummechanische moleculen gespot in supergeleidende apparaten  Een deeltje tegelijk een licht op donkere materie laten schijnen
Een deeltje tegelijk een licht op donkere materie laten schijnen Is chlorofluorocarbon oplosbaar in water, vervuilt het water?
Is chlorofluorocarbon oplosbaar in water, vervuilt het water?  Waarom is de omgeving belangrijk?
Waarom is de omgeving belangrijk?  Hoe heeft de wetenschap ons geholpen om een dieper inzicht in de wereld te hebben?
Hoe heeft de wetenschap ons geholpen om een dieper inzicht in de wereld te hebben?  Nieuwe vergelijkingen om de gestalte nauwkeuriger te schatten op basis van de lengte van het scheenbeen
Nieuwe vergelijkingen om de gestalte nauwkeuriger te schatten op basis van de lengte van het scheenbeen Kunnen de hersenen ‘niet-conventionele’ geometrieën (en abstracte ruimtes) in kaart brengen?
Kunnen de hersenen ‘niet-conventionele’ geometrieën (en abstracte ruimtes) in kaart brengen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

