
Wetenschap
Welke bindingen zijn polaire f-f o-o o-h-h-h?
* f-f (fluorine-fluorine): nonpolar
* Fluoratomen hebben dezelfde elektronegativiteit, wat betekent dat ze even elektronen aantrekken.
* De binding is symmetrisch en er is geen verschil in ladingsverdeling.
* O-O (Oxygen-Oxygen): nonpolar
* Net als F-F hebben zuurstofatomen dezelfde elektronegativiteit.
* De binding is symmetrisch.
* o-h (zuurstofhydrogen): Polar
* Zuurstof is veel elektronegatiefer dan waterstof.
* Dit creëert een gedeeltelijke negatieve lading (Δ-) op het zuurstofatoom en een gedeeltelijke positieve lading (Δ+) op het waterstofatoom.
* H-H (waterstof-hydrogen): nonpolar
* Waterstofatomen hebben dezelfde elektronegativiteit.
* De binding is symmetrisch.
Key Concept:Electronegativity
Elektronegativiteit is het vermogen van een atoom in een molecuul om elektronen aan te trekken. Hoe hoger het elektronegativiteitsverschil tussen twee gebonden atomen, hoe meer polair de binding.
 Waarom zou je chemie nodig hebben voor anesthesiologie?
Waarom zou je chemie nodig hebben voor anesthesiologie?  Is ferro sulfaat een anorganische verbinding?
Is ferro sulfaat een anorganische verbinding?  Wat is de meest voorkomende chemische lekkage?
Wat is de meest voorkomende chemische lekkage?  Hoe verschilt de relatieve dichtheid van water als vaste stof en vloeistof van die van de meeste andere stoffen?
Hoe verschilt de relatieve dichtheid van water als vaste stof en vloeistof van die van de meeste andere stoffen?  Welk type atomen worden in een skeletmodel een organisch molecuul getoond?
Welk type atomen worden in een skeletmodel een organisch molecuul getoond?
 Milieumicroben gebruiken om uranium uit grondwater te verwijderen
Milieumicroben gebruiken om uranium uit grondwater te verwijderen Juridische risico's van Keystone XL benadrukken de gevaren om investeerders voor klimaatverandering te plaatsen
Juridische risico's van Keystone XL benadrukken de gevaren om investeerders voor klimaatverandering te plaatsen Een wetenschappelijk mysterie oplossen en een oplossing vinden voor de industrie
Een wetenschappelijk mysterie oplossen en een oplossing vinden voor de industrie Wat is onkruidverspreiding?
Wat is onkruidverspreiding?  Literatuur werpt licht op de geschiedenis en het mysterie van de Zuidelijke Oceaan
Literatuur werpt licht op de geschiedenis en het mysterie van de Zuidelijke Oceaan
Hoofdlijnen
- Hoe weten cellen wanneer ze de celcyclus moeten doorlopen? Nieuwe studie vindt verband tussen verdeeldheid en groeisnelheid
- Geen levend fossiel:hoe de Coelacanth onlangs tientallen nieuwe genen heeft ontwikkeld
- Inheemse vissoorten lopen gevaar na verwijdering van water uit de Colorado-rivier
- Welk type natuurfenonenom wordt uitgelegd in Ceres Proserpina?
- Verschillen tussen "Fysiek" en "Fysiologisch"
- Studie kan strategieën opleveren om het goede cholesterol te verhogen
- Welke rol werd gespeeld door de glazen kralen in cellulair ademhalingsexperiment?
- Bij exocytose versmelt het membraanpakket met?
- Welke structuur in levende organismen is gemaakt van fosfolipiden?
- Groene theeverbinding helpt siRNA in cellen te glippen
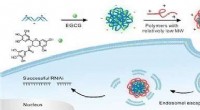
- Natuurkundigen meten moleculaire elektronische eigenschappen van vitamines

- Een nieuwe generatie kunstmatige netvliezen op basis van 2D-materialen

- Diepgaande leertechnieken leren het neurale model retrosynthese te spelen
- Nieuwe materialen van perovskiet dagen traditionele noties van hogedrukchemie uit

 Geconfronteerd met hoge smogniveaus, Milaan gaat auto's zondag verbieden
Geconfronteerd met hoge smogniveaus, Milaan gaat auto's zondag verbieden Wat is het verschil tussen een ruimtevaartuig en ruimteschip?
Wat is het verschil tussen een ruimtevaartuig en ruimteschip?  Het uitschakelen van de Niagarawatervallen zou inzicht kunnen opleveren over hoe watervallen canyons uitsnijden, zegt een expert
Het uitschakelen van de Niagarawatervallen zou inzicht kunnen opleveren over hoe watervallen canyons uitsnijden, zegt een expert  Zijn Web 2.0 Office-apps alleen maar bekabelde wiki's met rare namen?
Zijn Web 2.0 Office-apps alleen maar bekabelde wiki's met rare namen?  Hoe functie abrupt kan ontstaan of verdwijnen in fysieke en biologische systemen
Hoe functie abrupt kan ontstaan of verdwijnen in fysieke en biologische systemen  Het een oorlog tegen de wetenschap noemen heeft gevolgen
Het een oorlog tegen de wetenschap noemen heeft gevolgen Hoeveel gram koolstofdioxide wordt geproduceerd wanneer 23,5 g 1-heptanol reageert met overtollige zuurstof in een verbrandingsreactie?
Hoeveel gram koolstofdioxide wordt geproduceerd wanneer 23,5 g 1-heptanol reageert met overtollige zuurstof in een verbrandingsreactie?  Duiven beter in multitasken dan mensen:studie
Duiven beter in multitasken dan mensen:studie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

