
Wetenschap
Welke verbinding wordt geproduceerd wanneer 6,08 g stikstof combineert met 13,92 zuurstof?
1. Bepaal de mol van elk element:
* stikstof (n):
* Molaire massa van n =14,01 g/mol
* Mol n =6,08 g / 14,01 g / mol =0,434 mol
* zuurstof (O):
* Molaire massa van o =16,00 g/mol
* Mol O =13,92 g / 16,00 g / mol =0,870 mol
2. Vind de molverhouding:
* Deel de mol van elk element door het kleinste aantal mol (in dit geval 0,434 mol):
* N:0,434 mol / 0,434 mol =1
* O:0,870 mol / 0,434 mol ≈ 2
3. Bepaal de empirische formule:
* De molverhouding geeft aan dat de verbinding 1 stikstofatoom heeft voor elke 2 zuurstofatomen.
* De empirische formule is n₂o₄ , dat is dinitrogen tetroxide .
Belangrijke opmerking: Dinitrogene tetroxide is een zeer reactieve verbinding. In de echte wereld is het waarschijnlijk in evenwicht met stikstofdioxide (NO₂).
 Welke fijnstofverontreiniging vormt het grootste gezondheidsrisico?
Welke fijnstofverontreiniging vormt het grootste gezondheidsrisico? Kunstmatige intelligentie kan een revolutie teweegbrengen in waarschuwingen voor zee-ijs
Kunstmatige intelligentie kan een revolutie teweegbrengen in waarschuwingen voor zee-ijs Hoe zien Rattle Snake Dens eruit?
Hoe zien Rattle Snake Dens eruit?  De droge gebieden van Afrika krijgen meer steun. Hoe u hier het beste van kunt maken?
De droge gebieden van Afrika krijgen meer steun. Hoe u hier het beste van kunt maken? Welk fenomeen wordt gebruikt om de binnenkant van de aarde te bestuderen?
Welk fenomeen wordt gebruikt om de binnenkant van de aarde te bestuderen?
Hoofdlijnen
- Welke transcribeerreactantie wanneer ze worden geassocieerd met enzymen?
- Het decoderen van de cognitie van honden:machinaal leren geeft een glimp van hoe de hersenen van een hond weergeven wat hij ziet
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Een nieuwe strategie om cold case-onderzoeken te versnellen
- Hoe reproduceren parameciums zich?
- DNA-onderzoek van de beroemde Amerikaanse sledehond laat zien wat hem zo stoer maakte
- Een hybride bloem zou het genotype hebben?
- Wat is het cluster van cellen die een zich ontwikkelende ei omringen in eierstok genoemd?
- Rechts- of linkshandig? Genexpressie vertelt het verhaal van de evolutie van de slak
- Reinigen zonder te schrobben en chemicaliën te gebruiken. Wetenschappers ontwikkelen zelfreinigend aluminium oppervlak

- Onderzoekers simuleren het proces van lijmslijtage

- Wetenschappers onthullen de intercluster- en intraclusterdynamiek van met thiolaat beschermde goud-zilverlegeringen

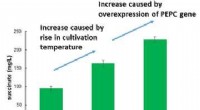
- 'S Werelds meest efficiënte productie van succinaat uit koolstofdioxide
- Zeewaterbacteriën bieden aanknopingspunten om melanoom te bestrijden
 Dagelijkse voorbeelden van situaties om kwadratische vergelijkingen toe te passen
Dagelijkse voorbeelden van situaties om kwadratische vergelijkingen toe te passen  Afbeelding:Hubble maakt een galactische potpourri van deeltjes
Afbeelding:Hubble maakt een galactische potpourri van deeltjes Veranderingen in jetstream kunnen extreme weersomstandigheden tegen 2060 versterken
Veranderingen in jetstream kunnen extreme weersomstandigheden tegen 2060 versterken Hoe is Egypte getroffen door de geografie ervan?
Hoe is Egypte getroffen door de geografie ervan?  Wat voor soort banden zal Amerika vormen?
Wat voor soort banden zal Amerika vormen?  De gevolgen van het coronavirus herleven het gesprek over een universeel basisinkomen
De gevolgen van het coronavirus herleven het gesprek over een universeel basisinkomen NASA-NOAA-satelliet toont omvang van Irmas-restanten
NASA-NOAA-satelliet toont omvang van Irmas-restanten Tencent koopt belang in Japans gamingbedrijf achter Elden Ring
Tencent koopt belang in Japans gamingbedrijf achter Elden Ring
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

