
Wetenschap
Wat wordt bedoeld met natriumacetaat een basiszout?
1. Hydrolyse van het anion:
- Natriumacetaat in oplossing dissocieert in natriumionen (Na+) en acetaationen (ch₃coo-).
- Het acetaation, de conjugaatbasis van een zwak zuur (azijnzuur, ch₃cooh), ondergaat hydrolyse in water.
- Het reageert met watermoleculen om hydroxide-ionen (OH-) en azijnzuur te produceren:
`` `
Ch₃coo⁻ + h₂o ⇌ ch₃cooh + oh⁻
`` `
- De productie van hydroxide -ionen maakt de oplossing basic.
2. pH van de oplossing:
- De hydrolyse van acetaationen leidt tot een toename van de hydroxide -ionenconcentratie, wat resulteert in een pH groter dan 7.
- Een pH groter dan 7 duidt op een basisoplossing.
3. Zout van sterke basis en zwak zuur:
- Natriumacetaat wordt gevormd uit de reactie van een sterke basis (natriumhydroxide, NaOH) en een zwak zuur (azijnzuur, ch₃cooh).
- Zouten gevormd uit een sterke basis en een zwak zuur zijn typisch eenvoudig.
Samenvattend:
Natriumacetaat wordt beschouwd als een eenvoudig zout vanwege de hydrolyse van zijn acetaatanion, dat hydroxide -ionen produceert en de pH van de oplossing verhoogt. De vorming van een basisoplossing is een kenmerk van zouten gevormd uit een sterke basis en een zwak zuur.
 Orkaan Chriss oog staart naar NASA's Aqua-satelliet
Orkaan Chriss oog staart naar NASA's Aqua-satelliet Een dampende ketel volgt de ondergang van de dinosauriërs
Een dampende ketel volgt de ondergang van de dinosauriërs Koolstofuitstoot en El Nino zorgen ervoor dat de oceanen recordtemperaturen bereiken
Koolstofuitstoot en El Nino zorgen ervoor dat de oceanen recordtemperaturen bereiken  Tropical Rain Forest Biome Landscape Kenmerken
Tropical Rain Forest Biome Landscape Kenmerken  Twee soorten golftreinen op gemiddelde breedtegraden leiden tot extreme hitte in Zuid-Korea en Zuid-centraal Japan
Twee soorten golftreinen op gemiddelde breedtegraden leiden tot extreme hitte in Zuid-Korea en Zuid-centraal Japan
Hoofdlijnen
- Freud en Oedipus:doet een van beide er nog toe?
- Ontwikkelen planten- en diercellen een celplaat?
- Uit onderzoek blijkt dat sommige bomen oververhit raken in warmere regenwouden
- Welke vakken studeren wetenschapper?
- Door het proces van meiose worden sekscellen geproduceerd die zijn?
- Wat betekent het als de wetenschap van het plaatsen van tings met vergelijkbare eigenschappen in groepen?
- Waarom de suikerkorrels een monster van de materie zijn. Welke reden?
- Hoe beïnvloeden milieuchemicaliën gieren?
- Ontdekking van structurele specialisatie in talloze eierstokken
- Nieuwe watersplitsingskatalysator kan het gemakkelijker maken om zonnebrandstof te genereren

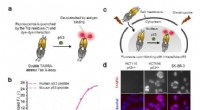
- Onderzoekers rapporteren over live intracellulaire beeldvorming met nieuwe, voorwaardelijk actieve immunofluorescentieprobe
- Hoe mosselen ijsvrij blijven in een ijskoude wereld

- Van de plaats delict naar de rechtszaal - de reis van een DNA-monster

- Van één uur tot één minuut:nieuwe analysetechniek vereenvoudigt het proces om bisfenol A-verontreinigingen te detecteren

 Waarom de ontdekking van het graf van Cleopatra de geschiedenis zou herschrijven
Waarom de ontdekking van het graf van Cleopatra de geschiedenis zou herschrijven  Het verschil tussen een stekelvarken en BMW?
Het verschil tussen een stekelvarken en BMW?  Geen olie- en gasgiganten die zich houden aan de klimaatdoelstellingen:rapport
Geen olie- en gasgiganten die zich houden aan de klimaatdoelstellingen:rapport  Neutronen wijzen de weg naar geoptimaliseerde crashtolerante auto's
Neutronen wijzen de weg naar geoptimaliseerde crashtolerante auto's Staat Thiamin op het periodieke tabel met elementen?
Staat Thiamin op het periodieke tabel met elementen?  Het proces van het omzetten van basiswetenschappelijke kennis in bruikbare producten wordt gebeld?
Het proces van het omzetten van basiswetenschappelijke kennis in bruikbare producten wordt gebeld?  Verbetering van de prestaties van metaal-organische raamwerkmaterialen
Verbetering van de prestaties van metaal-organische raamwerkmaterialen Wat zijn twee carrières waarbij biotechnologie betrokken is?
Wat zijn twee carrières waarbij biotechnologie betrokken is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

