
Wetenschap
Heeft NaCl een grotere roosterergie dan MGO?
* de wet van Coulomb: Roosterergie is recht evenredig met het product van de ladingen van de ionen en omgekeerd evenredig met de afstand daartussen.
* opladen: MGO heeft een hogere lading (mg²⁺ en o²⁻) in vergelijking met NaCl (Na⁺ en CL⁻). Dit betekent dat de elektrostatische aantrekkingskracht tussen ionen in MGO sterker is.
* ionische straal: Mg²⁺ en o²⁻ zijn kleinere ionen dan Na⁺ en Cl⁻. Dit betekent dat de afstand tussen de ionen in MGO kleiner is, wat leidt tot een sterkere elektrostatische aantrekkingskracht.
Samenvattend: De combinatie van hogere ladingen en kleinere ionische stralen in MGO resulteert in aanzienlijk grotere roosterergie in vergelijking met NaCl.
Hoofdlijnen
- Welke celvorm wordt beat aangepast voor de snelle beweging van stoffen van de ene naar de andere?
- Getrainde haviken schrikken kleinere vogels af, trek blikken in LA
- Uit onderzoek blijkt dat de mitochondriale fosfaatdrager een belangrijke rol speelt bij de virulentie van Candida albicans
- Waarom verplaatsen chloroplasten zich in Elodea?
- Ontsnapte GGO-canolaplanten blijven langdurig bestaan, maar verliezen mogelijk hun technische resistentie tegen pesticiden
- DNA-ontdekking kan licht werpen op zeldzame kinderziekte
- Organel dat water uit de cel pompt?
- Wat gebruiken wetenschappers om een systeem of een object te vertegenwoordigen?
- Tegelijkertijd inzoomen door tijd en ruimte met superresolutie om te begrijpen hoe cellen zich delen
- Studie onthult doorbreking van dansende barrière die kristalgroei regelt

- Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan

- Samenwerking levert veelbelovende innovatie op in vlekbestendigheid

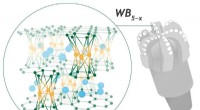
- Onderzoekers lossen 60 jaar oude puzzel op over superhard materiaal
- Geneesmiddelen en producten voor persoonlijke verzorging opzuigen uit water

 Hoe wordt de volgende fase van de menselijke evolutie genoemd?
Hoe wordt de volgende fase van de menselijke evolutie genoemd?  Hoe voorspel je genetische overerving met behulp van eenvoudige overerving?
Hoe voorspel je genetische overerving met behulp van eenvoudige overerving?  Wat zijn enkele echte toepassingen van trigonometrie?
Wat zijn enkele echte toepassingen van trigonometrie?  Is Venus de heetste planeet in het zonnestelsel?
Is Venus de heetste planeet in het zonnestelsel?  Wat is de vergelijking voor een reactie tussen ijzer en zoutzuur?
Wat is de vergelijking voor een reactie tussen ijzer en zoutzuur?  Simulaties laten zien hoe gentherapie effectiever kan worden gemaakt
Simulaties laten zien hoe gentherapie effectiever kan worden gemaakt  Focus op een lichtemitterende diode
Focus op een lichtemitterende diode Door SwRI geleide studie legt wetenschappelijke gegevens vast van Great American Eclipse
Door SwRI geleide studie legt wetenschappelijke gegevens vast van Great American Eclipse
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


