
Wetenschap
Wanneer kalium- en broomatomen chemische bindingen vormen, wat wordt geproduceerd?
Dit is waarom:
* kalium (k) is een metaal in groep 1 van de periodiek systeem. Het heeft één valentie -elektron, dat het gemakkelijk verliest om een stabiele elektronenconfiguratie te bereiken.
* bromine (br) is een niet -metaal in groep 17. Het heeft zeven valentie -elektronen en heeft er nog een nodig om een stabiele elektronenconfiguratie te bereiken.
Wanneer kalium en broom reageren, verliest kalium zijn valentie -elektron en vormt een positief geladen kaliumion (k+). Bromine wint dit elektron en vormt een negatief geladen bromide-ion (Br-). Deze tegengesteld geladen ionen trekken elkaar elektrostatisch aan en vormen een ionische binding. Deze ionische binding resulteert in de vorming van kaliumbromide (KBR), een witte kristallijne vaste stof.
 Hoe onvolledig is het fossielenbestand?
Hoe onvolledig is het fossielenbestand?  Faseovergangen in olivijn kunnen de oorzaak zijn van diepe seismische breuken
Faseovergangen in olivijn kunnen de oorzaak zijn van diepe seismische breuken De diepe Zuidelijke Oceaan is de sleutel tot intensere ijstijden
De diepe Zuidelijke Oceaan is de sleutel tot intensere ijstijden Studies tonen aan dat verstedelijking stormen en regenval ondanks de omgeving beïnvloedt
Studies tonen aan dat verstedelijking stormen en regenval ondanks de omgeving beïnvloedt  Europese oogstverliezen door hitte en droogte verdrievoudigd in 50 jaar:studie
Europese oogstverliezen door hitte en droogte verdrievoudigd in 50 jaar:studie
Hoofdlijnen
- Wat worden wetenschappelijke modellen gebruikt om een voorbeeld te geven van elk de volgende typen Idee Fysieke computer.?
- Wat is de wetenschappelijke naam van een herbivoor en een carnivoor?
- Zijn bacteriën een bron van restrictie -enzymen in DNA?
- Wat is de functie van een irisdiafragma op een microscoop?
- Welk organel in plantencellen zorgt ervoor dat ze voedsel kunnen maken?
- Wat zijn de 10 wetenschapstakken?
- Nieuwe drievoudige medicijncombinatie effectief tegen antibioticaresistente bacteriën
- Waar zijn gifstoffen en afval ontgiften in een cel?
- Kleine moleculen behouden stamcellen:Onderzoekers laten zien wat constante plantengroei mogelijk maakt
- Nieuwe technieken onderzoeken vitale en ongrijpbare eiwitten

- Gerichte evolutie van een designer-enzym met een onnatuurlijk katalytisch aminozuur
- Kleine moleculen kunnen de sleutel zijn tot het verbeteren van de efficiëntie van organische zonnecellen

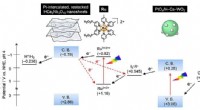
- Nieuwe fotokatalysator verhoogt de efficiëntie van watersplitsing voor schone waterstofproductie
- Sterk en kneedbaar Damascus-staal door additieve fabricage

 De hoogste partiële zuurstofdruk in de bloedsomloop
De hoogste partiële zuurstofdruk in de bloedsomloop Mooie toekomst voor gaN-nanodraden
Mooie toekomst voor gaN-nanodraden Wanneer is het belangrijk om een dictonaire te gebruiken?
Wanneer is het belangrijk om een dictonaire te gebruiken?  Wat zijn de vorming van rotsen als gevolg van geleidingsgeothermische energie binnen energie?
Wat zijn de vorming van rotsen als gevolg van geleidingsgeothermische energie binnen energie?  Braziliaans Amazonegebied registreert minste septemberbranden in 20 jaar
Braziliaans Amazonegebied registreert minste septemberbranden in 20 jaar Ruimtegemeenschap belooft terug te keren na Sojoez Mishap
Ruimtegemeenschap belooft terug te keren na Sojoez Mishap  Hoeveel kracht is er nodig om een sneeuwbal van 0,1 kg met een snelheid van 15 naar boven te bewegen?
Hoeveel kracht is er nodig om een sneeuwbal van 0,1 kg met een snelheid van 15 naar boven te bewegen?  Organellen die de plaats zijn van eiwitsynthese?
Organellen die de plaats zijn van eiwitsynthese?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

