Wetenschap
Welk type binding zal zich waarschijnlijk vormen van ijzer en zwavel?
* Elektronegativiteitsverschil: IJzer (Fe) heeft een elektronegativiteit van ongeveer 1,8, terwijl zwavel (s) een elektronegativiteit van ongeveer 2,5 heeft. Dit significante verschil in elektronegativiteit (ongeveer 0,7) geeft aan dat zwavel een sterkere aantrekkingskracht heeft op elektronen dan ijzer.
* elektronenoverdracht: Vanwege het elektronegativiteitsverschil zal zwavel de neiging hebben elektronen uit ijzer te krijgen. Deze elektronenoverdracht zal ertoe leiden dat ijzeren elektronen verliezen en een positief geladen ion worden (Fe²⁺), terwijl zwavel elektronen wint en een negatief geladen ion wordt (S²⁻).
* Ionische bindingsvorming: De elektrostatische aantrekkingskracht tussen de tegengesteld geladen ionen (Fe²⁺ en S²⁻) zal leiden tot de vorming van een ionische binding.
Daarom is de verbinding gevormd tussen ijzer en zwavel waarschijnlijk een ionische verbinding zoals ijzer (II) sulfide (FES) .
 Wat zijn de 2 soorten mengsels en hoe ze verschillen?
Wat zijn de 2 soorten mengsels en hoe ze verschillen?  Zachte en ionengeleidende kunsttong van hydrogel voor astringentieperceptie
Zachte en ionengeleidende kunsttong van hydrogel voor astringentieperceptie Hoe meng je 1 deel op 3 delen water?
Hoe meng je 1 deel op 3 delen water?  Hoe uraniumwinning werkt
Hoe uraniumwinning werkt  Katalysator gemaakt van ijzer kan een belangrijke reactie veroorzaken voor het maken van organische verbindingen
Katalysator gemaakt van ijzer kan een belangrijke reactie veroorzaken voor het maken van organische verbindingen
 Braziliaanse officier van justitie beveelt aan om Total-olievergunning in de buurt van Amazon te weigeren
Braziliaanse officier van justitie beveelt aan om Total-olievergunning in de buurt van Amazon te weigeren Door NASA ondersteunde tool versnelt natuurbrandherstel
Door NASA ondersteunde tool versnelt natuurbrandherstel Satellietgegevens voor de landbouw
Satellietgegevens voor de landbouw Indonesië begint met cloud seeding om bosbranden op afstand te houden
Indonesië begint met cloud seeding om bosbranden op afstand te houden Welke klimaatinnovaties zullen de opwarming van de aarde echt beperken?
Welke klimaatinnovaties zullen de opwarming van de aarde echt beperken?
Hoofdlijnen
- Geheimen van vetplanten water-wijs manieren onthuld
- Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin
- In welke cel is er geen verdeling?
- Welke naam wordt gegeven aan het organisme dat zich van afzonderlijke cellen tot vele soorten cellen ontwikkelt?
- Wat zorgt ervoor dat iemand man of vrouw wordt geboren?
- Hoe onderhoudt een cel homeostase?
- Wat is een meercellige massa die het embryo voedt totdat het zelfondersteunende zaailingen wordt?
- Heeft menselijke cellen een celmembraan?
- Wat is evolutie die zich voordoet gedurende een korte periode die wordt genoemd?
 Afbeelding:Hubble vindt een veld met sterren
Afbeelding:Hubble vindt een veld met sterren  Ammoniak breken:een nieuwe katalysator om bij lage temperaturen waterstof te maken uit ammoniak
Ammoniak breken:een nieuwe katalysator om bij lage temperaturen waterstof te maken uit ammoniak Wetenschappers ontwikkelen methode om functionele elementen van kwantumcomputers op te bouwen
Wetenschappers ontwikkelen methode om functionele elementen van kwantumcomputers op te bouwen Heeft fluor of broom een grotere waarde in ionische straal?
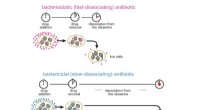
Heeft fluor of broom een grotere waarde in ionische straal?  Sterven bacteriën ooit uit? Nieuw onderzoek zegt ja, groots
Sterven bacteriën ooit uit? Nieuw onderzoek zegt ja, groots  Klimaatverandering en oceaanzuurstof:zuurstofarme zones zijn gekrompen tijdens warme perioden in het verleden, ontdekken wetenschappers
Klimaatverandering en oceaanzuurstof:zuurstofarme zones zijn gekrompen tijdens warme perioden in het verleden, ontdekken wetenschappers Lage verwachtingen weerhouden jonge mensen met een handicap om naar de universiteit te gaan
Lage verwachtingen weerhouden jonge mensen met een handicap om naar de universiteit te gaan Kunnen we redoxtitratie uitvoeren zonder verwarming?
Kunnen we redoxtitratie uitvoeren zonder verwarming?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com