
Wetenschap
Wat is de reactie waarbij waterstof wordt verbrand?
Hier is de chemische vergelijking:
2 H₂ (G) + O₂ (G) → 2 H₂o (G) + warmte
Verklaring:
* h₂ (g) vertegenwoordigt waterstofgas.
* o₂ (g) vertegenwoordigt zuurstofgas.
* h₂o (g) vertegenwoordigt waterdamp.
* warmte komt vrij, wat een exotherme reactie aangeeft.
Wat gebeurt er:
* Wanneer waterstofgas wordt blootgesteld aan een ontstekingsbron (zoals een vlam), reageert het met zuurstof in de lucht.
* Deze reactie combineert twee waterstofmoleculen (H₂) met één zuurstofmolecuul (O₂) om twee watermoleculen (H₂o) te vormen.
* Dit proces geeft een aanzienlijke hoeveelheid warmte en licht vrij, wat we waarnemen als de vlam van brandende waterstof.
Sleutelpunten:
* Waterstofverbranding is een zeer efficiënte reactie, waardoor veel energie per massa -eenheid van brandstof wordt geproduceerd.
* Het is een schone brandende brandstof en produceert alleen water als bijproduct, waardoor het een veelbelovend alternatief is voor fossiele brandstoffen.
* Het hanteren en opslaan van waterstofgas vereist echter speciale voorzorgsmaatregelen vanwege de zeer ontvlambare aard.
 Eerste proefvaarten van een revolutionaire nieuwe onderzeese robot
Eerste proefvaarten van een revolutionaire nieuwe onderzeese robot Laserkarteringsproject toont effecten van fysieke veranderingen in de droge valleien van Antarctica
Laserkarteringsproject toont effecten van fysieke veranderingen in de droge valleien van Antarctica Drie keer grotere reducties in de uitstoot van broeikasgassen in de VS dan eerder gemeld
Drie keer grotere reducties in de uitstoot van broeikasgassen in de VS dan eerder gemeld Gevolgen van bodemverontreiniging
Gevolgen van bodemverontreiniging  Evaluatie van op het land gebaseerde mitigatiestrategieën voor het bereiken van de klimaatdoelstellingen van 2°C
Evaluatie van op het land gebaseerde mitigatiestrategieën voor het bereiken van de klimaatdoelstellingen van 2°C
Hoofdlijnen
- Waarom vogels van een veer samen leken
- Studie onderstreept nieuwe strategieën om resistente bacteriën te bestrijden
- Hoe lang zou het duren voordat 2 bacteriecellen zich kunnen verdelen en in 4 cellen veranderen?
- Hoe een iconische foto van een appel de inspiratie vormde voor een verbeterde celanalyse
- Welke functie heeft het ademhalingssysteem?
- Interne factoren die van invloed zijn op celverdeling
- Wat gebeurt er met een diercel wanneer deze zich in een hypotone oplossing bevindt?
- Wat is de studie van ethische implicaties Biologisch onderzoek en toepassingen, vooral in veldgeneeskunde?
- Welke curve is hoogstwaarschijnlijk gegenereerd uit de analyse van een enzym in een menselijke maag onder sterk zure omstandigheden?
- Chemische detectiecellen helemaal opnieuw synthetiseren
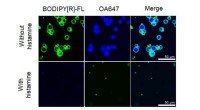
- Nieuwe methode voor het produceren van optische materialen verlaagt de kosten, verbetert de prestaties
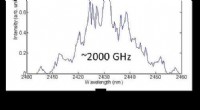
- Zullen de futures-superbatterijen van zeewater worden gemaakt?
- Wetenschappers ontwikkelen nieuwe aanpak om te voorspellen hoe vloeistoffen bevriezen

- Programmeren van Van der Waals-interacties met complexe symmetrieën in microdeeltjes met behulp van vloeibare kristalliniteit
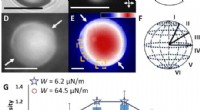
 Pleepering in hete klimaat Midden -Oosten?
Pleepering in hete klimaat Midden -Oosten?  Tijdigheid van betaling, promoties kunnen burgerschapsgedrag bij werknemers vergroten
Tijdigheid van betaling, promoties kunnen burgerschapsgedrag bij werknemers vergroten De klant centraal stellen is niet langer de beste marketingstrategie
De klant centraal stellen is niet langer de beste marketingstrategie Een volledig vrouwelijk ruimtewandelingduo richt zijn blik op de maan
Een volledig vrouwelijk ruimtewandelingduo richt zijn blik op de maan Actieve schietoefeningen op scholen kunnen meer kwaad dan goed doen
Actieve schietoefeningen op scholen kunnen meer kwaad dan goed doen Orkaan Katrina gaf voormalige gevangenen een nieuwe start in nieuwe steden:hoe meer mensen deze weg uit de misdaad te geven?
Orkaan Katrina gaf voormalige gevangenen een nieuwe start in nieuwe steden:hoe meer mensen deze weg uit de misdaad te geven? Welke kracht houdt de planeten in beweging?
Welke kracht houdt de planeten in beweging?  Convergente evolutie:wanneer een goed idee tussen soorten beweegt
Convergente evolutie:wanneer een goed idee tussen soorten beweegt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

