
Wetenschap
Waarom is de reactie SO2 H2O H2SO2 niet in balans?
De reactie die u hebt gegeven, So₂ + H₂o → H₂so₂, is niet in balans omdat het aantal zuurstofatomen aan de linkerkant van de vergelijking niet gelijk is aan het aantal zuurstofatomen aan de rechterkant.
Dit is waarom:
* Linkszijde: Er zijn 3 zuurstofatomen (1 in SO₂ en 2 in H₂o).
* rechterkant: Er zijn 2 zuurstofatomen (2 in H₂so₂).
Om deze vergelijking in evenwicht te brengen, moeten we de coëfficiënten voor de chemische formules aanpassen:
so₂ + h₂o → h₂so₃
Nu is de vergelijking in balans:
* Linkszijde: 3 zuurstofatomen
* rechterkant: 3 zuurstofatomen
De gebalanceerde vergelijking weerspiegelt de werkelijke reactie, waarbij zwaveldioxide (SO₂) reageert met water (H₂o) om zwavelzuur (H₂so₃) te vormen.
 Wat is het oxidatiegetal van ZnBr2?
Wat is het oxidatiegetal van ZnBr2?  Hoe de complexiteit van grensvlakchemie zich vertaalt in atmosferische veranderingen
Hoe de complexiteit van grensvlakchemie zich vertaalt in atmosferische veranderingen  Natuurkundige identificeert hoe elektronenkristallen smelten
Natuurkundige identificeert hoe elektronenkristallen smelten  smartphone, blockchain-technologieën om nieuwe grenzen te openen in de strijd tegen voedselfraude
smartphone, blockchain-technologieën om nieuwe grenzen te openen in de strijd tegen voedselfraude Kristallisatie kristalhelder gemaakt
Kristallisatie kristalhelder gemaakt
Hoofdlijnen
- Waarom eten we in Science Lab?
- Welke enkele cel reproduceert zich na de conceptie?
- Hoe pathogene bacteriën de slingers en pijlen van infectie doorstaan
- Welke wetenschapper ontdekte dat hitte ziektekiemen doodt?
- Waarom een microscoop bij de basis en arm dragen?
- Nieuw onderzoek onthult hoe vleermuishersenen zijn georganiseerd voor echolocatie en vlucht
- Wat zijn enkele organismen met één cellen?
- Is rijst een voorbeeld van epigeale kieming?
- Worden biologische groenten en fruit binnenkort goedkoper?
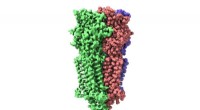
- Cryo-EM onthult structuur en mechanisme van de 5-HT3-receptor
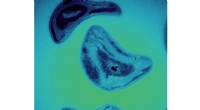
- Microbiële diefstal maakt afbraak van methaan mogelijk, giftige methylkwik
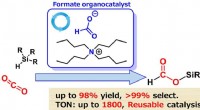
- Chemici ontdekken sleutel tot groenere voedselproductie

- Een metaalvrije, duurzame benadering van CO2-reductie
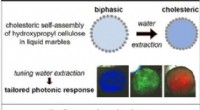
- Zelfassemblage van responsieve fotonische biobased materialen in vloeibare knikkers
 Het mysterie van het bewustzijn laat zien dat er mogelijk een grens is aan wat de wetenschap alleen kan bereiken
Het mysterie van het bewustzijn laat zien dat er mogelijk een grens is aan wat de wetenschap alleen kan bereiken  Huurlast drukt meer dan driekwart van de senioren met een laag inkomen in Californië, studie vondsten
Huurlast drukt meer dan driekwart van de senioren met een laag inkomen in Californië, studie vondsten Archeologen belichten oude culinaire praktijken met behulp van chemische biomarkers
Archeologen belichten oude culinaire praktijken met behulp van chemische biomarkers  Welk weefsel bevat jelly -achtig intercellulair materiaal?
Welk weefsel bevat jelly -achtig intercellulair materiaal?  Ingenieur ontdekt machtige kracht in kleine uitvinding op zonne-energie
Ingenieur ontdekt machtige kracht in kleine uitvinding op zonne-energie Zijn de wandaden van John James Audubon uit het verleden naar huis gekomen om te slapen?
Zijn de wandaden van John James Audubon uit het verleden naar huis gekomen om te slapen? Waarom zou een geoligest een analytische chemicus kunnen aarzelen om de mineralen in rots te identificeren?
Waarom zou een geoligest een analytische chemicus kunnen aarzelen om de mineralen in rots te identificeren?  Wanneer 2 continentale platen een vorm wijken.?
Wanneer 2 continentale platen een vorm wijken.?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

