
Wetenschap
De werkelijke molaire verhouding van elementen in een verbinding zoals uitgedrukt door de Subscripts -formule is wat?
Dit is waarom:
* Empirische formule: De eenvoudigste verhouding van het hele nummer van atomen van elk element in een verbinding. Het vertegenwoordigt de meest basale eenheid van de verbinding.
* Moleculaire formule: Het werkelijke aantal atomen van elk element in een molecuul van de verbinding. Dit kan hetzelfde zijn als de empirische formule of een veelvoud ervan.
Voorbeeld:
* Glucose: Moleculaire formule is c₆h₁₂o₆, empirische formule is ch₂o
In dit voorbeeld laat de moleculaire formule zien dat er 6 koolstof, 12 waterstof en 6 zuurstofatomen zijn in een glucosemolecuul. De empirische formule toont echter de eenvoudigste verhouding, die 1 koolstof, 2 waterstof en 1 zuurstof is.
Daarom vertegenwoordigen de subscripts in een formule rechtstreeks de empirische formule, die de werkelijke molaire verhouding van elementen in de verbinding is.
 Smeltende sneeuw bevat een giftige cocktail van verontreinigende stoffen
Smeltende sneeuw bevat een giftige cocktail van verontreinigende stoffen 5 redenen waarom parasieten gunstig zijn voor de aarde
5 redenen waarom parasieten gunstig zijn voor de aarde  De waarde van zeegras bij het veiligstellen van een duurzame planeet
De waarde van zeegras bij het veiligstellen van een duurzame planeet Zweden onthult nieuwe klimaatwet bekritiseert Trump
Zweden onthult nieuwe klimaatwet bekritiseert Trump Onderzoek toont aan dat rechtbanken kritisch zijn, ondergewaardeerde rol in klimaatbeleid
Onderzoek toont aan dat rechtbanken kritisch zijn, ondergewaardeerde rol in klimaatbeleid
Hoofdlijnen
- Hoe slangentanden evolueerden zodat ze perfect bij hun voedsel pasten
- Welke morfologische eigenschap maakt geen deel uit van het verdedigingsmechanisme in planten?
- Inleiding tot hoe gigantische virussen werken
- Welke evolutionaire betekenis geven wetenschappers deze in groene algen?
- Wat is een structuur in de kern waar RNA is getranscribeerd?
- Welke cellulaire organel wordt omgeven door een dubbel membraan bevat DNA en verantwoordelijk voor het omzetten van anorganische verbindingen in organisch met behulp van lichte energie?
- Hoe een moleculaire Superman het genoom beschermt tegen schade
- Studie identificeert knelpunten in vroege zeegrasgroei
- Moeten dieren stemrecht hebben?
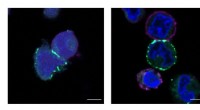
- Team verlicht de micro-omgeving, een nieuwe weg naar kankermedicijnen creëren
- Met koolstof gecoat nikkel maakt een waterstofbrandstofcel vrij van edele metalen

- Team lost tien jaar oud mysterie op in chemische transformaties

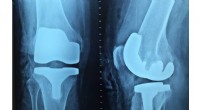
- Verbeterde reactie van het menselijk lichaam op implantaten
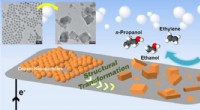
- Koperkatalysator zorgt voor een zeer efficiënte omzetting van CO2 naar brandstoffen
 Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen
Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen Wat is de energietransformatie bij een gashaard?
Wat is de energietransformatie bij een gashaard?  Waar theoretische fysica te bestuderen?
Waar theoretische fysica te bestuderen?  Contant geld nodig? Facebook breidt persoonlijke fondsenwervingstools uit
Contant geld nodig? Facebook breidt persoonlijke fondsenwervingstools uit  Welk deel van een atoom vind je protonen?
Welk deel van een atoom vind je protonen?  Waar is een meteoroïde als deze 75 km boven het oppervlak?
Waar is een meteoroïde als deze 75 km boven het oppervlak?  Wat is de molaire massa stikstofdioxide?
Wat is de molaire massa stikstofdioxide?  Als Yellowstone Volcano er is, wat zou er uitkomen?
Als Yellowstone Volcano er is, wat zou er uitkomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

