
Wetenschap
Vormen zwavel en zuurstof ionische verbindingen?
Dit is waarom:
* elektronegativiteit: Zuurstof is zeer elektronegatief, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Zwavel is ook elektronegatief maar minder dan zuurstof. Het verschil in elektronegativiteit tussen de twee elementen is niet groot genoeg om een volledige overdracht van elektronen te creëren, wat nodig is voor een ionische binding.
* Bonding Nature: In plaats van elektronen over te dragen, delen zwavel- en zuurstof elektronen om covalente bindingen te vormen. Dit delen creëert een stabielere opstelling voor beide atomen.
Voorbeelden van zwavel-zuurstofverbindingen zijn:
* zwaveldioxide (So₂)
* zwaveltrioxide (So₃)
* zwavelzuur (h₂so₄)
Deze verbindingen worden allemaal bij elkaar gehouden door covalente bindingen, geen ionische bindingen.
 Studie geeft aan hoe stof in het Midden-Oosten de zomermoessons op het Indiase subcontinent intensiveert
Studie geeft aan hoe stof in het Midden-Oosten de zomermoessons op het Indiase subcontinent intensiveert Klimaatverandering en de ineenstorting van Angkor Wat
Klimaatverandering en de ineenstorting van Angkor Wat Cellulosevezels zijn in opkomst als duurzame optie voor het verpakken van alles, van voedsel tot elektronica
Cellulosevezels zijn in opkomst als duurzame optie voor het verpakken van alles, van voedsel tot elektronica  Klimaatextremen in Australië:nieuw rapport analyseert grote gebeurtenissen in 2023
Klimaatextremen in Australië:nieuw rapport analyseert grote gebeurtenissen in 2023  Zoetwaterzoutvervuiling bedreigt ecosysteem en menselijke waterveiligheid
Zoetwaterzoutvervuiling bedreigt ecosysteem en menselijke waterveiligheid
Hoofdlijnen
- Wetenschappers ontdekken eiwitten die sperma helpen samensmelten met een eicel en vruchtbaarheidsbehandelingen kunnen verbeteren
- RNA en andere moleculen laten de kern door de structuur geroepen?
- Wat is interphase?
- Virussen leven en fokken in welke cellen?
- Welk proces brengen organismen kooldioxide terug naar de atmosfeer?
- Stamcelvaccins: de nieuwe grens in kankertherapie?
- 6 Leg uit waarom evolutie door natuurlijke selectie niet kan optreden als de variatie in een kenmerk bijdraagt aan verschillen in verschillen?
- Menselijke activiteit maakt het voor wetenschappers moeilijker om oceanen uit het verleden te interpreteren
- Wat wordt ingeschakeld door regulerende eiwitten?
- Team bewijst het concept van een natuurlijke benadering van anti-transpiranten

- Gezien de impact van de chemiecocktail voor binnenshuis

- Op maat gemaakte kunstmatige parelmoer

- Nieuwe chemische methode maakt het gemakkelijker om vervuilende pesticiden uit water te halen

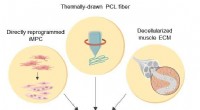
- Bioengineered hybride spiervezel voor regeneratieve geneeskunde
 Hoeveel versterkers van 3000 Watt op 220Volt AC enkele fase?
Hoeveel versterkers van 3000 Watt op 220Volt AC enkele fase?  Moleculen uit het water of de lucht filteren met nanomembranen
Moleculen uit het water of de lucht filteren met nanomembranen Wat zijn aardgashydraten?
Wat zijn aardgashydraten?  Kijkje op de Paris Air Show:gevechten met brede lichamen en drones (update)
Kijkje op de Paris Air Show:gevechten met brede lichamen en drones (update)  De snelheid waarmee energie wordt gebruikt?
De snelheid waarmee energie wordt gebruikt?  Een knuffel nodig tijdens de coronapandemie? Facebook heeft daar een nieuwe feelgood-reactie voor
Een knuffel nodig tijdens de coronapandemie? Facebook heeft daar een nieuwe feelgood-reactie voor Twee centimeter OS Welke fractie van een meter?
Twee centimeter OS Welke fractie van een meter?  Zijn jodium en water homogeen of heterogeen?
Zijn jodium en water homogeen of heterogeen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

