
Wetenschap
Welke van de volgende vergelijking van zwavelisotopen 32s en 35s?
* isotopen zijn atomen van hetzelfde element (in dit geval zwavel) die hetzelfde aantal protonen hebben maar verschillende aantallen neutronen.
* 32S heeft 16 protonen en 16 neutronen (32 - 16 =16).
* 35S heeft 16 protonen en 19 neutronen (35 - 16 =19).
Hier is een vergelijking:
* Atomisch nummer: Beide isotopen hebben hetzelfde atoomnummer (16), wat betekent dat ze beide zwavel zijn.
* Massienummer: 35S is zwaarder dan 32S omdat het nog drie neutronen heeft.
* chemische eigenschappen: Isotopen van hetzelfde element hebben zeer vergelijkbare chemische eigenschappen. Ze zullen op dezelfde manier reageren, maar sommige subtiele verschillen kunnen optreden vanwege het verschil in massa.
* stabiliteit: 32S is de meest stabiele isotoop van zwavel, terwijl 35S radioactief is en bèta -verval ondergaat.
Daarom is het belangrijkste verschil tussen 32S en 35S hun massa -aantal en stabiliteit. 35S is zwaarder en radioactief, terwijl 32S lichter en stabiel is.
 Niet-toxische vlamvertrager komt op de markt
Niet-toxische vlamvertrager komt op de markt Is H2O een zuur of alkali?
Is H2O een zuur of alkali?  Nieuwe zelf-assemblerende eiwithydrogels kunnen vele toepassingen voor biogeneeskunde bevatten
Nieuwe zelf-assemblerende eiwithydrogels kunnen vele toepassingen voor biogeneeskunde bevatten Wat is de eigenschap die een kwaliteit van substantie nooit verandert en kan worden gebruikt om de stof te identificeren?
Wat is de eigenschap die een kwaliteit van substantie nooit verandert en kan worden gebruikt om de stof te identificeren?  Hoe grijswaterterugwinning werkt
Hoe grijswaterterugwinning werkt
Hoofdlijnen
- Hoe werken organismen nuttige en schadelijke manieren op?
- 10 fascinerende feiten over de nieuwe levensboom-evolutiekaart
- Wat veroorzaakt slaap? Bij fruitvliegjes is het stress op cellulair niveau
- Waarom is DNA belangrijk voor het leven?
- Hoe diep gaat het leven? Studie beschrijft de microbiële buurt onder de oceaanbodem
- Wat is er van plastic gemaakt?
- Boomklimmende gekko's die smallere zitstokken gebruiken, hebben langere ledematen dan verwacht
- Een nieuw mechanisme voor hoe dierlijke cellen intact blijven
- Hoe nematoden de verdediging van ongedierte te slim af zijn
- Nieuwe moleculaire val reinigt meer radioactief afval van splijtstofstaven

- Vastleggen van het gedrag van katalysatoren met één atoom onderweg

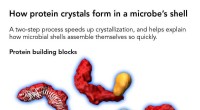
- Wetenschappers ontdekken hoe eiwitten kristallen vormen die een microbenomhulsel betegelen
- Neutronendiffractie-experimenten van materialen met structuren die meerdere metalen elementen bevatten

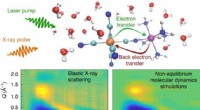
- Onderzoekers krijgen inzicht in hoe oplosmiddelmoleculen door licht gestuurde reacties beïnvloeden
 Wat gebeurt er als rotsen onder het aardoppervlak stress ondergaan?
Wat gebeurt er als rotsen onder het aardoppervlak stress ondergaan?  Toepassing van lichtgeschakelde magneten binnen handbereik
Toepassing van lichtgeschakelde magneten binnen handbereik GM wil Buick SUV vrijstellen van dreigende Trump-tarieven
GM wil Buick SUV vrijstellen van dreigende Trump-tarieven Hoe berekent wetenschapper de leeftijd van rots?
Hoe berekent wetenschapper de leeftijd van rots?  Genoommining leidt tot een nieuw type peptide-prenylatie
Genoommining leidt tot een nieuw type peptide-prenylatie Earth Microbiome Project:het microbioom van... alles in kaart brengen
Earth Microbiome Project:het microbioom van... alles in kaart brengen Gegroeid uit noodzaak:verticale landbouw neemt een vlucht in het vergrijzende Japan
Gegroeid uit noodzaak:verticale landbouw neemt een vlucht in het vergrijzende Japan De volgende stap is de lancering, terwijl Boeings Starliner een trektocht maakt naar Cape Canaveral
De volgende stap is de lancering, terwijl Boeings Starliner een trektocht maakt naar Cape Canaveral
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

