
Wetenschap
Hoe reageren sommige opgeloste stoffen op een oplosmiddel?
1. Oplossing:
* Polaire opgeloste stoffen in polaire oplosmiddelen: Dit is het klassieke geval van "Like Lost Like". Polaire opgeloste stoffen (zoals suiker of zout) lossen gemakkelijk op in polaire oplosmiddelen (zoals water). De sterke dipool-dipool-interacties tussen het oplosmiddel en de opgeloste moleculen leiden tot de vorming van oplossingsschalen, waardoor de opgeloste stof effectief uit elkaar wordt getrokken en zich over het oplosmiddel verspreidt.
* Niet-polaire opgeloste stoffen in niet-polaire oplosmiddelen: Evenzo lossen niet-polaire opgeloste stoffen (zoals olie of vetten) op in niet-polaire oplosmiddelen (zoals benzine). De zwakke Londense dispersiekrachten tussen de moleculen zijn voldoende om te mengen.
2. Interacties voorbij eenvoudige oplossing:
* ionische verbindingen in water: Ionische verbindingen zoals NaCl dissociëren in hun respectieve ionen (Na+ en Cl-) wanneer opgelost in water. De polaire watermoleculen omringen de ionen, vormen hydratatieschalen en houden ze gescheiden.
* zuren en basen: Zuren en basen ondergaan specifieke reacties met water, wat leidt tot de vorming van respectievelijk hydronium (H3O+) of hydroxide (OH-) ionen. Dit verandert de pH van de oplossing.
* Complexe vorming: Bepaalde opgeloste stoffen kunnen complexen vormen met de oplosmiddelmoleculen. Overgangsmetaalionen kunnen bijvoorbeeld complexen vormen met watermoleculen, waardoor de kleur van de oplossing wordt gewijzigd.
3. Onoplosbare opgeloste stoffen:
* olie en water: Olie en water mengen niet omdat de sterke waterstofbindingen in water veel sterker zijn dan de zwakke dispersiekrachten van Londen tussen olie- en watermoleculen. Dit leidt tot een scheiding van fasen.
Factoren die de oplosbaarheid beïnvloeden:
* Temperatuur: Over het algemeen verhoogt de toenemende temperatuur de oplosbaarheid voor de meeste vaste stoffen en gassen.
* Druk: Druk beïnvloedt de oplosbaarheid van gassen, waardoor de oplosbaarheid toeneemt naarmate de druk toeneemt.
* Aard van de opgeloste stof en oplosmiddel: Zoals hierboven vermeld, spelen de polariteit en andere eigenschappen van de opgeloste stof en oplosmiddelen een belangrijke rol.
Key Concepts:
* polariteit: Verwijst naar de verdeling van lading binnen een molecuul. Polaire moleculen hebben een positief en negatief einde, terwijl niet-polaire moleculen een meer gelijkmatige verdeling van lading hebben.
* intermoleculaire krachten: De krachten van aantrekkingskracht tussen moleculen. Hoe sterker de krachten, hoe groter de kans dat een opgeloste stof in een oplosmiddel oplost.
* Solvation: Het proces van opgeloste moleculen wordt omringd door oplosmiddelmoleculen.
Inzicht in de interacties tussen opgeloste stoffen en oplosmiddelen is cruciaal op vele gebieden, waaronder chemie, biologie en engineering. Het helpt ons het gedrag van oplossingen te voorspellen, nieuwe materialen te ontwerpen en biologische processen te begrijpen.
 Wat is het verschil tussen een homogeen en heterogeen mengsel?
Wat is het verschil tussen een homogeen en heterogeen mengsel?  Ontdek hoe cocaïne werkt
Ontdek hoe cocaïne werkt  Wat is de eenvoudigste vorm van chemische vergelijking voor zelfionisatiewater?
Wat is de eenvoudigste vorm van chemische vergelijking voor zelfionisatiewater?  Hoeveel equivalente Lewis-structuren zijn nodig om de binding in BrO4 te beschrijven?
Hoeveel equivalente Lewis-structuren zijn nodig om de binding in BrO4 te beschrijven?  Wat bevat meer waterstofionen Windex of Maalox?
Wat bevat meer waterstofionen Windex of Maalox?
 Welke rol speelt het milieu bij het definiëren van het uiterlijk van een organisme?
Welke rol speelt het milieu bij het definiëren van het uiterlijk van een organisme?  Agroforestry-systemen kunnen een cruciale rol spelen bij het tegengaan van klimaatverandering
Agroforestry-systemen kunnen een cruciale rol spelen bij het tegengaan van klimaatverandering Afval of schat? Gezinnen en hun geliefde bezittingen
Afval of schat? Gezinnen en hun geliefde bezittingen  Wat is het woord aardbeving in verschillende talen?
Wat is het woord aardbeving in verschillende talen?  Nieuwe metingen van breukzones kunnen ons helpen om subductie-aardbevingen te begrijpen
Nieuwe metingen van breukzones kunnen ons helpen om subductie-aardbevingen te begrijpen
Hoofdlijnen
- Wat is een niet-voorbeeld van de wetenschappelijke theorie?
- Wat is een giganthropithicus?
- Is pectine een monomeer of polymeer?
- Welke micro -organismen hebben geen kern in hun cellen?
- Chimpansees ontdekken aanwijzingen over het menselijk verleden?
- Bacteriën reprodelen door welk proces?
- Volgens Lamarck evolueerde soorten?
- Wat betekent M in de wetenschap?
- Waar zijn plantes van gemaakt?
- Ingrediënt in Indiase lange peper veelbelovend tegen hersenkanker in diermodellen
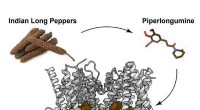
- Eerste gedetailleerde blik op cruciaal enzym bevordert kankeronderzoek

- Koud sinteren produceert condensatormateriaal bij record lage temperaturen

- Nieuwe chemie maakt verbeteringen aan magische medicijnen gemakkelijker

- Van kantoorramen tot Mars:wetenschappers debuteren superisolerende gel

 Renault, Fiat Chrysler in gesprek
Renault, Fiat Chrysler in gesprek Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie
Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie Drie generaties gegevens laten zien hoe rijke (blanke) gezinnen rijk blijven
Drie generaties gegevens laten zien hoe rijke (blanke) gezinnen rijk blijven Kometen instortende kliffen en stuiterende rotsblokken
Kometen instortende kliffen en stuiterende rotsblokken Proton-kern-smashups leveren aanwijzingen op over quark-gluon-plasma
Proton-kern-smashups leveren aanwijzingen op over quark-gluon-plasma Nieuw materiaal kan ademhalingsdruppels uit de lucht verwijderen
Nieuw materiaal kan ademhalingsdruppels uit de lucht verwijderen Great Barrier Reef-koralen kunnen de opwarming van de aarde nog een eeuw overleven
Great Barrier Reef-koralen kunnen de opwarming van de aarde nog een eeuw overleven Wat chimpansees ons kunnen leren over economie
Wat chimpansees ons kunnen leren over economie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

