
Wetenschap
Wat bevat watermoleculen en de waterstofbindingen tussen de de meeste levensondersteunende eigenschappen uitleggen?
Dit is waarom:
* Watermoleculen: Water (H₂o) bestaat uit twee waterstofatomen en één zuurstofatoom. Deze atomen zijn verbonden door covalente bindingen, die sterk zijn en elektronen delen.
* Waterstofbindingen: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (nabij de hydrogenen) en een enigszins negatief uiteinde (nabij de zuurstof). Met deze polariteit kunnen watermoleculen zwakke bindingen vormen die waterstofbruggen met elkaar worden genoemd. Deze bindingen zijn zwakker dan covalente bindingen, maar ze zijn nog steeds belangrijk.
* Levensvoorzienende eigenschappen: De unieke eigenschappen van water die het leven ondersteunen, zijn grotendeels te wijten aan de waterstofbindingen tussen watermoleculen:
* Hoge warmtecapaciteit: Water kan veel warmte -energie absorberen voordat de temperatuur aanzienlijk toeneemt. Dit helpt om de temperatuur van organismen en de omgeving te reguleren.
* Hoge verdampingswarmte: Water vereist veel energie om van een vloeistof naar een gas te veranderen (verdamping). Dit helpt organismen af te koelen door zweten.
* Uitstekend oplosmiddel: Met de polariteit van het water kan het veel stoffen oplossen, waardoor het een ideaal medium is voor chemische reacties in levende organismen.
* cohesie en hechting: Waterstofbindingen geven water zijn samenhangende (plakken bij elkaar) en lijm (vasthouden aan andere oppervlakken) eigenschappen. Hierdoor kan water door planten en dieren bewegen.
* Dichtheid: Water is minder dicht als een vaste stof (ijs) dan als een vloeistof. Dit betekent dat ijs op het water is voor het waterleven.
Samenvattend, het vermogen van water om waterstofbindingen te vormen, is de sleutel tot zijn unieke eigenschappen die het essentieel maken voor het leven.
 Nieuwe inzichten in het faalmechanisme van lithium-ionbatterijen
Nieuwe inzichten in het faalmechanisme van lithium-ionbatterijen Waarom veranderen planten zonlicht CO2 en water in suikerzuurstof?
Waarom veranderen planten zonlicht CO2 en water in suikerzuurstof?  Een diepe variatie-autoencoder voor proteomics-massaspectrometriegegevensanalyse
Een diepe variatie-autoencoder voor proteomics-massaspectrometriegegevensanalyse  Wat is de juiste formule voor Mn iv fosfaatfosfaation PO4 3?
Wat is de juiste formule voor Mn iv fosfaatfosfaation PO4 3?  Hoeveel is 5 milliliter vloeistoffen?
Hoeveel is 5 milliliter vloeistoffen?
Hoofdlijnen
- Welke microscoop wordt gebruikt voor het observeren van gistmitochondriën?
- Hoe verschilt het ene eiwit van een ander eiwit?
- Wat is de moleculaire formule voor wijnstokken?
- Wat maakt een held?
- Hoe vissers profiteren van de omgekeerde evolutie van kabeljauw
- Wat betekent het als je zegt dat wetenschap een cyclus is?
- Wat is metrologhy de wetenschap van?
- Wetenschappers moeten begrijpen hoe de ontwikkeling van kieuwen de groei van vissen beperkt
- Welk bouwsteen is het belangrijkste structurele materiaal van organismen?
- Palladiumkatalysator versnelt twee afzonderlijke reacties, bruikbare moleculen maken in één proces
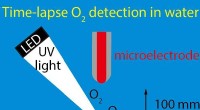
- Snellere detectie van door fotokatalysatoren gegenereerde zuurstof heeft grote gevolgen voor schone energie
- Moleculair in kaart brengen gemakkelijk gemaakt

- Schudden, rammelaar, en rol naar hoogrenderende fotovoltaïsche energie
- Ingenieurs ontwikkelen recept om kogelvrije vesten drastisch te versterken

 Onzekere klimaattoekomst kan energiesystemen verstoren
Onzekere klimaattoekomst kan energiesystemen verstoren Hoe te berekenen Audpc
Hoe te berekenen Audpc  Wanneer chemisch werk wordt gedaan door een organisme, wat gebeurt er met de gegenereerde warmte?
Wanneer chemisch werk wordt gedaan door een organisme, wat gebeurt er met de gegenereerde warmte?  Welke stad is 39 graden North Latitude en 90 West Loogte?
Welke stad is 39 graden North Latitude en 90 West Loogte?  Hoe de I-90 in Washington veiliger werd voor wilde dieren, chauffeurs
Hoe de I-90 in Washington veiliger werd voor wilde dieren, chauffeurs  Wat is het verschil tussen atomen, elementenverbindingen en moleculen?
Wat is het verschil tussen atomen, elementenverbindingen en moleculen?  Takken van de aardewetenschap en hun betekenis?
Takken van de aardewetenschap en hun betekenis?  Wat is de moleculaire formule van relatieve massa 72?
Wat is de moleculaire formule van relatieve massa 72?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

