
Wetenschap
Welke combinaties van elementen in een verbinding zouden moleculair zijn?
Inzicht in moleculaire verbindingen
* Covalente binding: Moleculaire verbindingen worden gevormd door covalente bindingen. In deze bindingen delen atomen * elektronen om een stabiele elektronenconfiguratie te bereiken.
* niet -metalen: Moleculaire verbindingen worden typisch gevormd tussen niet -metalen. Dit komt omdat niet -metalen meestal vergelijkbare elektronegativiteitswaarden hebben (de neiging om elektronen aan te trekken).
generalisaties
* twee niet -metalen: Elke combinatie van twee of meer niet -metalen zal resulteren in een moleculaire verbinding. Voorbeelden:
* H₂o (water)
* Co₂ (koolstofdioxide)
* NH₃ (ammoniak)
* Ch₄ (methaan)
* waterstof met een niet -metaal: Waterstof gedraagt zich vaak als een niet -metaal en vormt moleculaire verbindingen met niet -metalen.
* Uitzonderingen: Er zijn enkele uitzonderingen met metalloïden (elementen die eigenschappen van metalen en niet -metalen delen). Siliciumdioxide (SIO₂) is bijvoorbeeld een netwerk solide, geen moleculaire verbinding.
Key Takeaways
* Zoek naar combinaties van niet -metalen.
* Waterstof werkt vaak als een niet -metaal in deze verbindingen.
* Let op uitzonderingen met metalloïden.
Laat het me weten als je specifieke voorbeelden wilt of de uitzonderingen in meer detail wilt verkennen!
 Wie wordt een held? Het is meer dan alleen een persoonlijkheidskenmerk
Wie wordt een held? Het is meer dan alleen een persoonlijkheidskenmerk  Wat wordt bedoeld met uitsterven?
Wat wordt bedoeld met uitsterven?  Overstromingen, regen verplettert New Orleans voorafgaand aan potentiële orkaan
Overstromingen, regen verplettert New Orleans voorafgaand aan potentiële orkaan De belangrijkste factor die de snelheid van verwering bepaalt, is type rots en?
De belangrijkste factor die de snelheid van verwering bepaalt, is type rots en?  Canadezen sterven sneller in gebieden met meer luchtvervuiling
Canadezen sterven sneller in gebieden met meer luchtvervuiling
Hoofdlijnen
- Waarom zijn gekke wormen een potentieel probleem of uitdaging voor onze ecosystemen?
- Onderzoekers identificeren virusresistentiegen van wild gras voor verbetering van graangewassen
- AI kan onderzoekers helpen begrijpen wat virussen van plan zijn in de oceanen en in uw darmen
- Kinesins negeren zwakke krachten omdat ze zware lasten dragen
- Wat is vergelijkende biochemie?
- Naar welk gezin behoort Beryllium?
- Kan ruimte ons helpen onze cellen te begrijpen?
- Waar is de locatie van alle nucleïnezuren?
- Wat is een betrouwbare bron van wetenschappelijke informatie?
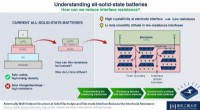
- Glashelder maken:kristalliniteit vermindert de weerstand in volledig solid-state batterijen
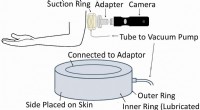
- Nieuw apparaat kan littekens bij cosmetische chirurgie helpen verminderen
- Medewerkers van de röntgenfaciliteit van Berkeley Labs mobiliseren zich om COVID-19-gerelateerd onderzoek te ondersteunen

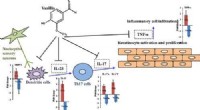
- Psoriasis voorkomen met vanilline
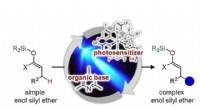
- Selectieve vorming van koolstof-koolstofbindingen mogelijk maken op de inherent inerte positie van enolsilylethers
 Wat is het kenmerk van Dwarf Planet?
Wat is het kenmerk van Dwarf Planet?  Wat zijn de vier beweging?
Wat zijn de vier beweging?  Welke heeft een grotere massa een veer van twee inch of één gum?
Welke heeft een grotere massa een veer van twee inch of één gum?  Hoe beïnvloedt de mantel van de aarde andere secties?
Hoe beïnvloedt de mantel van de aarde andere secties?  Welk vuurwerk bevat metalen die helder gekleurd zijn als ze worden verbrand. Ze zijn minder reactief dan andere. Welk metaal is daar een voorbeeld van?
Welk vuurwerk bevat metalen die helder gekleurd zijn als ze worden verbrand. Ze zijn minder reactief dan andere. Welk metaal is daar een voorbeeld van?  Jaagden mosasauriërs als orka's?
Jaagden mosasauriërs als orka's? Kun je me een voorbeeldzin geven voor het woord verkennen?
Kun je me een voorbeeldzin geven voor het woord verkennen?  Op welke invalshoek trekt zonnestraling in polaire gebieden de aarde?
Op welke invalshoek trekt zonnestraling in polaire gebieden de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

