
Wetenschap
Als 81,7 ml 1,34 M HnO3 werd gebruikt om 56.3 te titreren, vindt u een LIOH -oplossing de concentratie lithiumhydroxide?
1. Schrijf de gebalanceerde chemische vergelijking:
Hno₃ (aq) + liOH (aq) → lino₃ (aq) + h₂o (l)
2. Bepaal de mol Hno₃:
* Molariteit (m) =mol (mol) / volume (l)
* Herschikken om op te lossen voor mol:mol =m * v
* Converteer het volume hno₃ van ml naar l:81,7 ml * (1 l / 1000 ml) =0,0817 l
* Bereken de mol Hno₃:1,34 m * 0,0817 L =0,1096 Mol Hno₃
3. Gebruik de molverhouding van de gebalanceerde vergelijking:
* De gebalanceerde vergelijking toont een 1:1 molverhouding tussen HNO₃ en LIOH. Dit betekent dat 0,1096 mol HNO₃ reageerde met 0,1096 mol LIOH.
4. Bereken de concentratie van LIOH:
* Concentratie (m) =mol (mol) / volume (l)
* Converteer het volume van liOH van ml naar l:56,3 ml * (1 l / 1000 ml) =0,0563 l
* Bereken de concentratie van LIOH:0.1096 mol / 0,0563 L = 1,95 m
Daarom is de concentratie van de lithiumhydroxide -oplossing 1,95 m.
 Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media
Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media  Uit welke elementen bestaat natriumhypochloriet?
Uit welke elementen bestaat natriumhypochloriet?  Een nieuwe strategie voor een groener gebruik van calciumcarbide
Een nieuwe strategie voor een groener gebruik van calciumcarbide Kunnen een kation en anion iso -elektronisch zijn uit dezelfde periode?
Kunnen een kation en anion iso -elektronisch zijn uit dezelfde periode?  Drukken maakt polymeren plat, verbetering van elektrische en optische eigenschappen
Drukken maakt polymeren plat, verbetering van elektrische en optische eigenschappen
 Wil jij niet mijn buurman zijn? Huizenjacht is een strijd voor paren van gemengd ras met kinderen
Wil jij niet mijn buurman zijn? Huizenjacht is een strijd voor paren van gemengd ras met kinderen  Hoe terrorisme onze houding beïnvloedt
Hoe terrorisme onze houding beïnvloedt  Verborgen in Afrikaanse diamanten, meer dan een miljard jaar geschiedenis van de diepe aarde
Verborgen in Afrikaanse diamanten, meer dan een miljard jaar geschiedenis van de diepe aarde De strijd tegen de opwarming van de aarde en klimaatverandering vereist een brede energieportfolio
De strijd tegen de opwarming van de aarde en klimaatverandering vereist een brede energieportfolio Waarom één volwassen straatboom behouden veel beter is voor mens en natuur dan veel nieuwe planten
Waarom één volwassen straatboom behouden veel beter is voor mens en natuur dan veel nieuwe planten
Hoofdlijnen
- Wie heeft de regels van embryonale ontwikkeling gegeven?
- Lianen, bomen vertonen een gevarieerde stam-xyleemstructuur-functie-link
- Fycologen ontdekken waardoor sommige bruine algen glinsteren en andere niet
- Hoe wordt Arabidopsis gebruikt in plantonderzoek?
- Wat is replicatie van een studie?
- Wat is vergelijkende biochemie?
Vergelijkende biochemie kan een vaag begrip zijn met meerdere betekenissen, alhoewel het boeiende interacties tussen organismen en hun biologieën kan onthullen. Op zijn minst noemen wetenschappers het een interdiscip
- Welke krachten vormen de Eaths -kenmerken?
- Wat moet ik doen als ik een eenzame, gezellige walvisachtige tegenkom?
- Kunnen kikkererwtengenen mosterdzaad redden van de ziekte?
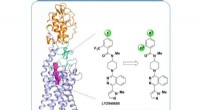
- Wetenschappers ontcijferen het multi-domein, volledige structuur van de humane smoothened receptor
- Varkensvlees in wezen vrij van residuen van diergeneesmiddelen

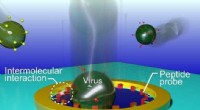
- Nieuwe virale identificatiemethode ontwikkeld
- Geavanceerde biomaterialen met zijde-fibroïne-bioactief glas om patiëntspecifieke 3D-bottransplantaten te ontwikkelen

- Supraballs bieden een nieuwe manier om materialen te kleuren

 Wat worden 2 organellen alleen aangetroffen in dierlijke cellen?
Wat worden 2 organellen alleen aangetroffen in dierlijke cellen?  Noord-NSW is geen onbekende voor overstromingen, maar deze was anders
Noord-NSW is geen onbekende voor overstromingen, maar deze was anders Warme wind:nieuw inzicht in wat de Antarctische ijsplaten verzwakt
Warme wind:nieuw inzicht in wat de Antarctische ijsplaten verzwakt Baanbrekende studie opent de deur naar bredere biomedische toepassingen voor Raman-spectroscopie
Baanbrekende studie opent de deur naar bredere biomedische toepassingen voor Raman-spectroscopie Adidas verhoogt winstvooruitzichten na sterk kwartaal
Adidas verhoogt winstvooruitzichten na sterk kwartaal Onderzoek naar klimaatverandering van de achteruitgang van de jongen van lederschildpadden levert geen antwoorden op
Onderzoek naar klimaatverandering van de achteruitgang van de jongen van lederschildpadden levert geen antwoorden op DYNAMO behaalt eerste waarneming van het ladingsscheidingseffect
DYNAMO behaalt eerste waarneming van het ladingsscheidingseffect Op de 2D-schaal, isotopensamenstelling heeft onvoorziene effecten op lichtemissie
Op de 2D-schaal, isotopensamenstelling heeft onvoorziene effecten op lichtemissie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

