
Wetenschap
Industriële toepassingen van gemeenschappelijk ioneneffect?
1. Neerslag en scheiding:
* Selectieve neerslag: Het gemeenschappelijke ioneneffect staat centraal in het proces van selectieve neerslag, waarbij een specifiek ion uit een oplossing wordt neergeslagen terwijl andere opgelost blijven. Dit wordt veel gebruikt in analytische chemie voor het scheiden en identificeren van verschillende ionen. In de kwalitatieve analyse van metaalkationen kan de toevoeging van een gemeenschappelijk ionen zoals chloride of sulfide bijvoorbeeld selectief specifieke metaalionen neerslachten, wat helpt bij hun identificatie.
* Afvalwaterzuivering: Bij afvalwaterzuivering wordt het gemeenschappelijke ioneneffect gebruikt om zware metalen zoals lood, kwik en cadmium te verwijderen. Door een gemeenschappelijk ion te introduceren, zoals sulfaat of sulfide, neemt de oplosbaarheid van deze zware metaalionen af, wat leidt tot hun neerslag en verwijdering uit het afvalwater.
2. Controle van oplosbaarheid en ontbinding:
* kristalgroei en kristallisatie: In de gecontroleerde groei van kristallen voor verschillende toepassingen (elektronica, geneesmiddelen, optica) speelt het gemeenschappelijke ioneneffect een cruciale rol. Door de concentratie van een gemeenschappelijk ion zorgvuldig aan te passen, kan de snelheid van kristalgroei en de uiteindelijke kristalgrootte nauwkeurig worden geregeld.
* Corrosiebestrijding: Bij corrosiepreventie kan het gemeenschappelijke ioneneffect worden gebruikt om de oplosbaarheid van metaalionen die bijdragen aan corrosie te verminderen. Door bijvoorbeeld chromaationen aan een watersysteem toe te voegen, wordt de oplosbaarheid van ijzerionen verminderd, waardoor de vorming van roest wordt geremd.
3. Analytische chemie en titratie:
* Titratie -analyse: Het gemeenschappelijke ioneneffect wordt toegepast in titratie -analyse, met name in neerslagtitraties. Door een bekende oplossing te gebruiken van een reagens dat een gemeenschappelijk ion bevat, kan de concentratie van een onbekende oplossing precies worden bepaald. De concentratie van chloride -ionen in een monster kan bijvoorbeeld worden bepaald door te titreren met een standaard zilvernitraatoplossing, waarbij zilverionen werken als het gemeenschappelijke ion, waardoor de neerslag van zilverchloride veroorzaakt.
4. Industriële processen:
* metallurgie: Bij de extractie van metalen uit hun ertsen wordt het gemeenschappelijke ioneneffect gebruikt om de oplosbaarheid van metaalionen aan te passen tijdens uitloog- en zuiveringsprocessen. Door de concentratie van gewone ionen te regelen, kan de efficiëntie van metaalextractie worden verbeterd.
* textielindustrie: Het kleurstofproces is vaak gebaseerd op het gewone ioneneffect om de opname van kleurstof door vezels te regelen. Het toevoegen van gemeenschappelijke ionen aan het kleurstofbad kan de oplosbaarheid van de kleurstof verminderen, waardoor de naleving van de vezels wordt verbeterd.
* Farmaceutische industrie: Het gemeenschappelijke ioneneffect wordt gebruikt bij de ontwikkeling van farmaceutische formuleringen om de oplosbaarheid van medicijnmoleculen te regelen en hun absorptie en biologische beschikbaarheid te verbeteren.
5. Milieutoepassingen:
* Bodemsanering: Het gemeenschappelijke ioneneffect kan worden gebruikt om giftige metaalionen uit vervuilde grond te verwijderen. Door een geschikt gemeenschappelijk ion toe te voegen, neemt de oplosbaarheid van de giftige metaalionen af, wat leidt tot hun neerslag en immobilisatie in de bodem.
* Waterbehandeling: Bij waterbehandeling wordt het gemeenschappelijke ioneneffect gebruikt om calcium- en magnesiumionen te verwijderen (die hardheid veroorzaken) door carbonaationen toe te voegen om ze te neerslachten als respectievelijk calciumcarbonaat en magnesiumcarbonaat.
Over het algemeen heeft het gemeenschappelijke ioneneffect significante praktische toepassingen in verschillende industrieën, wat een krachtig hulpmiddel biedt voor het beheersen van chemische reacties, het scheiden van stoffen en het manipuleren van oplosbaarheid om de gewenste resultaten te bereiken.
 Wat gebeurt er als je broom en natrium mengt?
Wat gebeurt er als je broom en natrium mengt?  Hoeveel mol Mg is 2,01 keer 10x22 atomen?
Hoeveel mol Mg is 2,01 keer 10x22 atomen?  Kan een stabiele verbinding worden gemaakt van lithium en zuurstof?
Kan een stabiele verbinding worden gemaakt van lithium en zuurstof?  Welk type elektronen heeft een negatief geladen atoom?
Welk type elektronen heeft een negatief geladen atoom?  Waarom doen atomen zoals koolstof en stikstof om geen ionen te maken terwijl natriumchloor?
Waarom doen atomen zoals koolstof en stikstof om geen ionen te maken terwijl natriumchloor?
 lawines, een bergbedreiging
lawines, een bergbedreiging Bepaalt de hoeveelheid regen die in een gebied valt welke soorten organismen daar kunnen leven en waarom?
Bepaalt de hoeveelheid regen die in een gebied valt welke soorten organismen daar kunnen leven en waarom?  Waarom hebben bladeren in dezelfde plant verschillende maten?
Waarom hebben bladeren in dezelfde plant verschillende maten?  Wat zijn de vijf dingen van materie in wetenschappelijke namen?
Wat zijn de vijf dingen van materie in wetenschappelijke namen?  Sleutel voor irrigatiebeheer voor de productie van bio-energie om klimaatverandering tegen te gaan
Sleutel voor irrigatiebeheer voor de productie van bio-energie om klimaatverandering tegen te gaan
Hoofdlijnen
- Wat is een bijestinfectie?
- Je telefoon is een kiemfabriek, dus stop ermee om hem naar het toilet te brengen
- Vier hoofdelementen gevonden in een levend organisme?
- Hoe organiseren wetenschappers bestaande wetenschappelijke informatie?
- Wat te doen bij een hondenaanval en waarom ze postbodes zo haten
- Parasitaire wormen wachten niet om te worden opgeslokt door nieuwe gastheren
- Welk stadium mitose is het wanneer chromosomen verkorten en dikker worden, begint het nucleaire membraan te verdwijnen?
- Hoe plantensensoren ziekteverwekkers detecteren
- Waarom cellen de doorgang van ziekten toestaan
- Onderzoekers ontdekken methode om kalkaanslag te voorkomen

- Onderzoekers melden nieuw begrip van thermo-elektrische materialen

- Lab produceert eenvoudige fluorescerende oppervlakteactieve stoffen
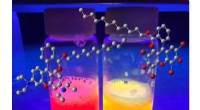
- Nieuw elektrodeontwerp kan leiden tot krachtigere batterijen
- Het wegnemen van de knelpunten in de prestaties van lithium-zwavelbatterijen

 Waarom we moeten heroverwegen wat we weten over stof
Waarom we moeten heroverwegen wat we weten over stof  Hoe een Sharknado zou werken
Hoe een Sharknado zou werken  Het bijhouden van de voortgang van kinderen met leren, taalstoornissen
Het bijhouden van de voortgang van kinderen met leren, taalstoornissen Overtuigende politiek:waarom emotionele beats rationeel zijn om contact te maken met kiezers
Overtuigende politiek:waarom emotionele beats rationeel zijn om contact te maken met kiezers Hoe oude bijenholen leidden tot een beter begrip van de Neanderthalers
Hoe oude bijenholen leidden tot een beter begrip van de Neanderthalers  Wetenschappers breiden geheugeneffectbereik uit door ruimtelijke filtering
Wetenschappers breiden geheugeneffectbereik uit door ruimtelijke filtering Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen
Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen Maakt Thanksgiving Turkije je echt slaperig?
Maakt Thanksgiving Turkije je echt slaperig?
Als je Thanksgiving-ritueel gepaard gaat met flauwvallen op de bank na een maaltijd, weet je al dat een feest met alles erop en eraan je moe maakt. Maar ondertekende de kalkoen je enkeltje naar snoozevil
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

