
Wetenschap
Wat wordt gebruikt om de specifieke warmtecapaciteit van een stof te vinden?
c =q / (m * Δt)
Waar:
* c is de specifieke warmtecapaciteit (gemeten in j/g ° C of cal/g ° C)
* Q is de hoeveelheid warmte -energie die wordt geabsorbeerd of afgegeven door de stof (gemeten in joules of calorieën)
* M is de massa van de stof (gemeten in gram)
* Δt is de temperatuurverandering van de stof (gemeten in ° C)
Hier is hoe u de specifieke warmtecapaciteit experimenteel kunt vinden:
1. Verhit de stof: U kunt de stof verwarmen met een warmtebron zoals een bunsenbrander of een hete plaat.
2. Metel de begintemperatuur: Gebruik een thermometer om de initiële temperatuur van de stof te registreren vóór het verwarmen.
3. Meet de eindtemperatuur: Nadat u de stof hebt verwarmd, neemt u de eindtemperatuur vast die deze bereikt.
4. Bereken de temperatuurverandering (Δt): Trek de begintemperatuur af van de eindtemperatuur.
5. Bereken de hoeveelheid warmte -energie (Q): U kunt een calorimeter gebruiken (een apparaat dat warmte -uitwisseling meet) om de hoeveelheid warmte te bepalen die wordt geabsorbeerd of vrijgegeven door de stof. Als alternatief, als u de kracht van de warmtebron kent en de tijd die deze is toegepast, kunt u q berekenen met behulp van de formule q =vermogen * tijd.
6. Meet de massa (m) van de stof.
7. Sluit de waarden aan op de formule: Gebruik de waarden die u hebt verzameld voor Q, M en AT om de specifieke warmtecapaciteit (C) van de stof te berekenen.
Voorbeeld:
Stel dat u 100 gram water verwarmt van 20 ° C tot 30 ° C en u bepaalt dat het water opgenomen 4184 joulen warmte -energie.
* Q =4184 J
* m =100 g
* Δt =30 ° C - 20 ° C =10 ° C
De formule gebruiken:
C =q / (m * Δt) =4184 j / (100 g * 10 ° C) = 4.184 J / g ° C
Dit is de specifieke warmtecapaciteit van water.
Opmerking:
* De specifieke warmtecapaciteit van een stof varieert afhankelijk van de toestand van de stof (vaste, vloeistof of gas).
* Het is belangrijk om variabelen zoals warmteverlies voor de omgeving te regelen om nauwkeurige resultaten te krijgen.
 Lage dosering, constant druppelen:vervuiling door farmaceutische en persoonlijke verzorging heeft invloed op het waterleven
Lage dosering, constant druppelen:vervuiling door farmaceutische en persoonlijke verzorging heeft invloed op het waterleven Senaatswetsvoorstel geprezen als mijlpaal voor klimaatbestrijding. Dit is wat je moet weten.
Senaatswetsvoorstel geprezen als mijlpaal voor klimaatbestrijding. Dit is wat je moet weten. Lijst met insecten die dood vlees eten
Lijst met insecten die dood vlees eten  Brand in Spanje bij Werelderfgoed onder controle
Brand in Spanje bij Werelderfgoed onder controle Ziektedragende muggen zeldzaam in ongestoorde tropische bossen
Ziektedragende muggen zeldzaam in ongestoorde tropische bossen
Hoofdlijnen
- Microevolution vs Macroevolution: Similiarities & Differences
- Zijn het echte wetenschappers niet moeten experimenten herhalen om te zien of thir -gegevens reproduceerbaar zijn?
- Waarom is stikstof belangrijk voor levende wezens?
- Welke massa omvat spieren vitale weefselsorganen en bot?
- Ondanks de wet stijgt het aantal doden door loodvergiftiging in New Hampshire
- Hoe signaalmoleculen voor de vorming van verschillende celtypen worden aangestuurd
- CRISPR-dragende nanodeeltjes bewerken het genoom
- Op welke manier controleert de samenleving de wetenschap?
- Waarom Hydrolyse lactose niet hydrolyseert?
- Een lasertechniek blijkt effectief om materiaal terug te winnen dat is ontworpen om industriële producten te beschermen

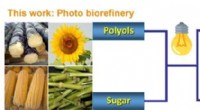
- Nieuwe fotokatalytische methode zet biopolyolen en suikers om in methanol en syngas
- Op weg naar een betere batterij:wetenschappers ontdekken de bron van degradatie in natriumbatterijen
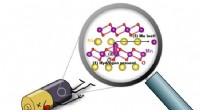
- Nieuwe techniek zet ammoniak naadloos om in groene waterstof

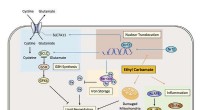
- Wetenschappers ontdekken het mechanisme voor ethylcarbamaat-geïnduceerde toxiciteit in gefermenteerd voedsel
 Hoe reproduceren de sprinkhanen?
Hoe reproduceren de sprinkhanen?  Wat zijn terrestrische fenomenen?
Wat zijn terrestrische fenomenen?  Wat is een enkel helixmolecuul?
Wat is een enkel helixmolecuul?  Leeft er een zanddollar?
Leeft er een zanddollar?  Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte
Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte Heeft Apollo 8 het ruimteschip op de maan geland?
Heeft Apollo 8 het ruimteschip op de maan geland?  Zijn virussen de nieuwe grens voor astrobiologie?
Zijn virussen de nieuwe grens voor astrobiologie? Wat beschrijft het beste de periode van een golf?
Wat beschrijft het beste de periode van een golf?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

