
Wetenschap
Wat helpt bepalen of een oplossing zuur of basic is?
1. pH -schaal
* De pH -schaal varieert van 0 tot 14, met:
* 0-6: Zuur
* 7: Neutraal (zoals zuiver water)
* 8-14: Basic (ook wel alkalisch genoemd)
* PH meten:
* Litmus -papier: Wordt rood in zure oplossingen, blauw in basisoplossingen.
* pH -meter: Biedt een numerieke lezing van de pH.
* indicatoren: Bepaalde chemicaliën veranderen van kleur, afhankelijk van de pH.
2. De aanwezigheid van ionen
* zuren Laat waterstofionen (H+) vrij wanneer opgelost in water.
* bases Laat hydroxide-ionen (OH-) vrij wanneer opgelost in water.
* Neutrale oplossingen hebben ongeveer gelijke hoeveelheden H+ en OH-.
3. Andere kenmerken
* zuren: Proef zuur, reageer met metalen om waterstofgas te produceren en kan blauw lakmoespapier rood worden.
* Bases: Smaak vaak bitter, voel je glad en kan rood lakmoespapier blauw worden.
Key Concepts
* Sterke zuren en basen: Volledig ioniseren in water, wat betekent dat ze al hun H+ of OH-ionen vrijgeven.
* Zwakke zuren en basen: Gedeeltelijk ioniseren in water.
Voorbeeld:
* azijn is zuur omdat het azijnzuur bevat, dat H+ -ionen vrijgeeft wanneer het in water wordt opgelost.
* bakpoeder is basic omdat het natriumbicarbonaat bevat, dat oh-ionen vrijgeeft wanneer het in water wordt opgelost.
Laat het me weten als je specifieke voorbeelden wilt verkennen of verdere uitleg nodig hebt!
 Moeten we een film maken waar het publiek van geniet of moeten we een Oscar-nominatie binnenhalen? Onderzoek onthult de logica van studio's
Moeten we een film maken waar het publiek van geniet of moeten we een Oscar-nominatie binnenhalen? Onderzoek onthult de logica van studio's  Waarom worden de termarische vlekken rood als ze in wasmiddel worden gedrenkt?
Waarom worden de termarische vlekken rood als ze in wasmiddel worden gedrenkt?  Heeft silicadioxide een lading?
Heeft silicadioxide een lading?  Eerste flexibele geheugenapparaat dat ferro-elektrisch materiaal van oxide gebruikt
Eerste flexibele geheugenapparaat dat ferro-elektrisch materiaal van oxide gebruikt Hoe Celsius converteren naar Kelvin
Hoe Celsius converteren naar Kelvin
 Is een lommerige zeedragonplant of dier?
Is een lommerige zeedragonplant of dier?  Te dichtbij of te ver? Wat fruitvliegjes ons leren over persoonlijke ruimte
Te dichtbij of te ver? Wat fruitvliegjes ons leren over persoonlijke ruimte  Indoor HEPA-filters verminderen de vervuiling binnenshuis aanzienlijk wanneer de buitenlucht ongezond is, studie vondsten
Indoor HEPA-filters verminderen de vervuiling binnenshuis aanzienlijk wanneer de buitenlucht ongezond is, studie vondsten Australische onderzoekers laten de evolutie van de bloemkleur zien, aangedreven door de voorkeuren van bijen
Australische onderzoekers laten de evolutie van de bloemkleur zien, aangedreven door de voorkeuren van bijen  Canadese ijskernmonsters tonen aan dat de temperaturen in het Holoceen hoger waren dan vandaag
Canadese ijskernmonsters tonen aan dat de temperaturen in het Holoceen hoger waren dan vandaag
Hoofdlijnen
- Waarom zijn vitamines belangrijk voor enzymen en hoe heet deze relatie?
- De zwaarste schildpad ter wereld? Overlevende van 8 keert terug naar oceaan
- Uit onderzoek blijkt dat menselijk geluid een negatieve invloed heeft op de overleving en voortplanting van krekels
- Wat zijn de functies van longblaasjes in de longen?
- Waarom is UV-licht schadelijk?
- Grootschalig scherm laat zien hoe talloze signaalroutes elkaar kruisen in het primaire eiwitverwerkingscentrum van de cel
- Hoe planten genetische herinneringen doorgeven
- Welke term verwijst naar de wetenschappelijke naamgeving van organismen waarin een tweedelige Latijnse naam het geslacht en de soort aangeeft?
- Wat is het belangrijkste domein van het leven?
- Video:De explosieve gevolgen van koeienboeren

- Nieuwe geconsolideerde bio-saccharificatietechniek voor lignocelluloseconversie ontwikkeld
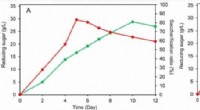
- Voorbehandelen van hinderlijke groenalgen met loog, ureum verhoogt bacteriële productie van biogas

- Hoe wetenschappers infectieveroorzakende biofilms bestrijden
- Onderzoekers sporen nieuwe biokatalysatoren op

 Besties op de werkplek:hoe u relaties op het werk kunt opbouwen terwijl u professioneel blijft
Besties op de werkplek:hoe u relaties op het werk kunt opbouwen terwijl u professioneel blijft  Computer uit Oekraïne betrokken bij aanslag op verkiezingen in Tennessee
Computer uit Oekraïne betrokken bij aanslag op verkiezingen in Tennessee Welke twee functies maken DNA tot een heel speciaal molecuul?
Welke twee functies maken DNA tot een heel speciaal molecuul?  Afbeeldingen laten zien dat het zonnezeil van het Lightsail 2-ruimtevaartuig is uitgezet
Afbeeldingen laten zien dat het zonnezeil van het Lightsail 2-ruimtevaartuig is uitgezet  De mysterieuze D-laag van de aarde:een overblijfsel van oude oceanen en planetaire botsingen
De mysterieuze D-laag van de aarde:een overblijfsel van oude oceanen en planetaire botsingen  Wat is de versnelling van een blok van 50 kg waarop een kracht van 500 N wordt uitgeoefend?
Wat is de versnelling van een blok van 50 kg waarop een kracht van 500 N wordt uitgeoefend?  Onderzoekers ontdekken de fysieke oorsprong van elektronische fasescheidingsverschijnselen in complexe oxiden
Onderzoekers ontdekken de fysieke oorsprong van elektronische fasescheidingsverschijnselen in complexe oxiden Hoe de zon asteroïden in onze buurt beïnvloedt
Hoe de zon asteroïden in onze buurt beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

