
Wetenschap
Welk effect heeft een katalysator?
1. Versnelt reacties: De primaire functie van een katalysator is om de snelheid van een chemische reactie te verhogen zonder in het proces te worden geconsumeerd. Het doet dit door een alternatieve reactieroute te bieden met een lagere activeringsenergie.
2. Lagere activeringsenergie: Activeringsenergie is de minimale hoeveelheid energie die nodig is voor reactanten om een reactie te starten. Katalysatoren bereiken dit door:
* het bieden van een oppervlak voor reactanten om te interageren: Dit brengt de reactanten dichter bij elkaar, waardoor ze gemakkelijker kunnen botsen en reageren.
* Tijdelijk bindend aan reactanten: Dit kan de banden in de reactanten verzwakken, waardoor ze gevoeliger zijn voor het breken en het vormen van nieuwe bindingen.
3. Heeft geen invloed op het evenwicht: Terwijl een katalysator de snelheid van een reactie versnelt, heeft het geen invloed op de evenwichtspositie van de reactie. Dit betekent dat het niet de relatieve hoeveelheden producten en reactanten in evenwicht verandert.
4. Zeer specifiek: Katalysatoren zijn vaak sterk specifiek op de reacties die ze beïnvloeden. Een katalysator die is ontworpen voor de ene reactie kan weinig of geen effect hebben op de andere.
5. Voorbeelden:
* Enzymen in biologische systemen zijn katalysatoren die biochemische reacties versnellen.
* Katalysatoren in de katalysator van een auto helpen schadelijke verontreinigende stoffen om te zetten in minder schadelijke gassen.
* Katalysatoren in de chemische industrie zijn cruciaal voor productieprocessen zoals de productie van kunststoffen, meststoffen en brandstoffen.
Samenvattend:
Katalysatoren zijn krachtige hulpmiddelen waarmee chemische reacties sneller en efficiënter kunnen plaatsvinden. Ze zijn essentieel op verschillende gebieden, van biologie en geneeskunde tot industrie en milieuwetenschappen.
 Heeft snelle zeespiegelstijging fossiele koraalriffen rond Hawaï verdronken?
Heeft snelle zeespiegelstijging fossiele koraalriffen rond Hawaï verdronken? Warm water verhoogde het aantal grote orkaan in 2017, studie zegt:
Warm water verhoogde het aantal grote orkaan in 2017, studie zegt: Zal de sneeuw van maart de kersenbloesems van Washington verpesten?
Zal de sneeuw van maart de kersenbloesems van Washington verpesten? NOAA-satellieten hebben in 2016 307 levens gered
NOAA-satellieten hebben in 2016 307 levens gered Hoe invasief onkruid bosbranden heter en frequenter kan maken
Hoe invasief onkruid bosbranden heter en frequenter kan maken
Hoofdlijnen
- Lijst van aseksueel reproducerende organismen
- Volledig geautomatiseerde detectierobot bevordert efficiënt grondonderzoek
- Prehistorische soa's kunnen de reden zijn waarom mensen monogaam werden
- Welke belangrijke functie hebben nucleïnezuren in een cel?
- Braziliaanse onderzoekers ontdekken zes nieuwe soorten zijdemiereneter
- Waarom sommige vissen 'junk' zijn en andere beschermd. Onderzoek wijst op vooroordelen tegen inheemse soorten
- Welke roept agroup van cellen die zich ontwikkelt uit een enkele originele cel?
- Welk element heeft slechts 4 protronen in de kern?
- Welke aanpassingen hebben ghaf-bomen?
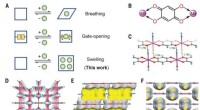
- Een mangaanpolymeer gebruiken om xyleenisomeren te scheiden
- C. elegans rondwormen oogsten een essentieel co-enzym uit de bacteriën die ze consumeren

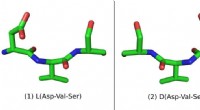
- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
- Hot brew koffie heeft een hoger gehalte aan antioxidanten dan cold brew

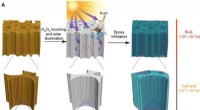
- Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas
 Moleculaire motor:vier rotatietoestanden
Moleculaire motor:vier rotatietoestanden Zijn alle planeet rond de zon draaien?
Zijn alle planeet rond de zon draaien?  Biodistributie van selenium benadrukt ontwikkelingsblootstellingsrisico's
Biodistributie van selenium benadrukt ontwikkelingsblootstellingsrisico's Kan de aarde worden beïnvloed als de helderheid van de zon verandert?
Kan de aarde worden beïnvloed als de helderheid van de zon verandert?  Wat is de naam voor het proces van scheiding 2 vloeistoffen?
Wat is de naam voor het proces van scheiding 2 vloeistoffen?  Niemand achterlaten geeft een paternalistische benadering van ontwikkeling weer
Niemand achterlaten geeft een paternalistische benadering van ontwikkeling weer Is er iets aan de hand met stinkend opblaasbaar zwembadspeelgoed?
Is er iets aan de hand met stinkend opblaasbaar zwembadspeelgoed? Hersentemperatuur kan nu worden gemeten met behulp van licht
Hersentemperatuur kan nu worden gemeten met behulp van licht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

