
Wetenschap
Wat gebeurt er met het inpakken van moleculen als water van ijswater verandert?
* ijs: In ijs zijn watermoleculen gerangschikt in een zeer geordende, kristallijne structuur. Elk molecuul vormt vier waterstofbindingen met zijn buren, waardoor een ruim, open rooster ontstaat. Deze roosterstructuur maakt ijs minder dicht dan vloeibaar water.
* vloeibaar water: Wanneer ijs smelt, beginnen de waterstofbindingen te breken, waardoor de moleculen dichter bij elkaar kunnen komen en minder worden geordend. De moleculen kunnen nu vrij rondlopen en een kleiner volume bezetten, wat leidt tot een toename van de dichtheid.
Hier is een vereenvoudigde analogie:
Zie ijs als een stel mensen die in een zeer georganiseerde lijn staan, hand in hand (waterstofbindingen) vasthouden en veel ruimte tussen hen achterlaten. Wanneer het ijs smelt, beginnen mensen handen los te laten en meer vrij te bewegen, waardoor ze dichter bij elkaar kunnen pakken.
Sleutelpunten:
* Dichtheid: Vloeibaar water is dichter dan ijs, daarom zweeft ijs.
* Waterstofbindingen: Het breken en hervormen van waterstofbindingen is cruciaal voor de overgang tussen ijs en vloeibaar water.
* Bestel: Vloeibaar water heeft een minder geordende structuur dan ijs.
Laat het me weten als je meer informatie wilt over een van deze punten!
 Nog geen oponthoud voor het door overstromingen geteisterde zuiden van Brazilië
Nog geen oponthoud voor het door overstromingen geteisterde zuiden van Brazilië  Ecologische landroof:voedsel versus brandstof versus bossen
Ecologische landroof:voedsel versus brandstof versus bossen Mensen leren als soort te denken
Mensen leren als soort te denken NASA heeft geïnvesteerd in het kraken van de koolstofpuzzel van de aarde
NASA heeft geïnvesteerd in het kraken van de koolstofpuzzel van de aarde Klimaatslachtoffers zoeken gerechtigheid, in de rechtszaal en op straat
Klimaatslachtoffers zoeken gerechtigheid, in de rechtszaal en op straat
Hoofdlijnen
- Biologen tonen aan dat de enige 'longloze' kikkersoort inderdaad longen heeft
- Waarom produceert kernsplijting peervormige kernen?
- Spechten vertonen tekenen van mogelijke hersenbeschadiging, maar dat is misschien geen slechte zaak
- Wat zouden de gevolgen van een mutatie die het lichaam verhinderde membraaneiwit te maken dat nodig is voor actief transportsuikerverteringssysteem?
- Wat is vooringenomenheid en hoe vermijd je het in de wetenschap?
- Waarom veranderen theorieën of hypothese in de wetenschap?
- Anatomie en fysiologie van een synapsenstructuur
- Wat is het evolutiemechanisme?
- Welke drie dingen zijn nodig om fotosynthese te laten plaatsvinden?
- Ingenieurs maken een eenvoudige test die stresshormonen in zweet kan meten, bloed, urine of speeksel

- Betere katalysatoren voor een duurzame bio-economie

- Onderzoekers maken van plastic flessenafval ultralicht supermateriaal met brede toepassingen

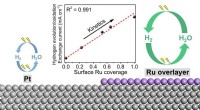
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
- Vliegen injecteren met slakkengif kan ons helpen moleculen te ontdekken voor het ontwikkelen van nieuwe medicijnen

 Wanneer was Pluto dichter bij de zon dan Neptunus?
Wanneer was Pluto dichter bij de zon dan Neptunus?  Hoe aardverschuivingen werken
Hoe aardverschuivingen werken  Had Jupiter bezoeken van de aarde?
Had Jupiter bezoeken van de aarde?  Respecteer inheemse voorouders:geleerden dringen aan op gemeenschapsbetrokkenheid vóór onderzoek
Respecteer inheemse voorouders:geleerden dringen aan op gemeenschapsbetrokkenheid vóór onderzoek Is er elke dag een volle maan van het jaar?
Is er elke dag een volle maan van het jaar?  Wat zijn de stikstofverbindingen met oxidatietoestanden?
Wat zijn de stikstofverbindingen met oxidatietoestanden?  Wat is kouder -5 graden Celsius of -16 graden Celsius?
Wat is kouder -5 graden Celsius of -16 graden Celsius?  Waarom blijven moderne astronomen de hemelse sfeer gebruiken als ze weten dat sterren niet allemaal op dezelfde afstand zijn?
Waarom blijven moderne astronomen de hemelse sfeer gebruiken als ze weten dat sterren niet allemaal op dezelfde afstand zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

