
Wetenschap
Zijn er chemische bindingen ontstaan wanneer valentie -elektronen worden gedeeld tussen atomen?
* Covalente bindingen worden gevormd wanneer valentie -elektronen worden gedeeld tussen atomen. Met dit delen kunnen beide atomen een stabielere elektronenconfiguratie bereiken, zoals die van een edelgas.
Hier is een uitsplitsing:
* valentie -elektronen: Dit zijn de elektronen in de buitenste schaal van een atoom, die betrokken zijn bij chemische binding.
* Elektronen delen: Wanneer twee atomen valentie -elektronen delen, creëren ze een gedeeld elektronenpaar dat wordt aangetrokken door beide atomaire kernen. Deze aantrekkingskracht houdt de atomen bij elkaar in een covalente binding.
Er zijn verschillende soorten covalente bindingen, afhankelijk van het aantal gedeelde elektronen:
* enkele binding: Een gedeeld paar elektronen
* Dubbele binding: Twee gedeelde paren elektronen
* Triple Bond: Drie gedeelde paren elektronen
Voorbeelden van covalente bindingen zijn:
* water (h₂o): Elk waterstofatoom deelt één elektron met het zuurstofatoom en vormt twee enkele bindingen.
* koolstofdioxide (co₂): Het koolstofatoom deelt twee elektronen met elk zuurstofatoom en vormt twee dubbele bindingen.
Laat het me weten als u dieper in de soorten covalente bindingen wilt verdiepen of meer vragen wilt hebben!
 Team ontwikkelt een elektrochemische methode om uranium te winnen, en mogelijk andere metaalionen, van oplossing
Team ontwikkelt een elektrochemische methode om uranium te winnen, en mogelijk andere metaalionen, van oplossing Welke twee subatomaire deeltjes bevinden zich in de atoomkern?
Welke twee subatomaire deeltjes bevinden zich in de atoomkern?  Kunnen we het vermogen van een plant om geneeskrachtige stoffen te synthetiseren benutten?
Kunnen we het vermogen van een plant om geneeskrachtige stoffen te synthetiseren benutten?  Wat is de naam C2H2O2?
Wat is de naam C2H2O2?  Onderzoekers demonstreren nieuwe manieren om selectiviteit voor biomarkers in bio-elektronica te bereiken
Onderzoekers demonstreren nieuwe manieren om selectiviteit voor biomarkers in bio-elektronica te bereiken
 Onderzoek verlengt lengte van gletsjer- en sneeuwgrensanalyse
Onderzoek verlengt lengte van gletsjer- en sneeuwgrensanalyse Onderzoekers lossen het vormingsmechanisme van sferische carbonaatconcreties op
Onderzoekers lossen het vormingsmechanisme van sferische carbonaatconcreties op Arctische toendra stoot meer methaan uit tijdens de herfstvorst dan tijdens de dooi in de lente
Arctische toendra stoot meer methaan uit tijdens de herfstvorst dan tijdens de dooi in de lente Een betere planning kan het stedelijk hitte-eilandeffect verminderen
Een betere planning kan het stedelijk hitte-eilandeffect verminderen Stormen veroorzaakten in 2016 enorm verlies van zee-ijs op Antarctica
Stormen veroorzaakten in 2016 enorm verlies van zee-ijs op Antarctica
Hoofdlijnen
- Een reeks gevouwen membranen die materialen in de cel verplaatsen?
- Wie doet de wetenschap?
- Wat eenzame slakken ons kunnen vertellen over de effecten van stress op het geheugen
- Welke organel zou je vinden in plantencellen maar geen dierlijke cellen?
- Waarom is ademhaling belangrijk voor een cel?
- Wat is de Griekse oorsprong van de levenstheorie?
- Vermeld de functie van elke organel?
- Elementen van nucleïnezuren
- Wat betekent substraten?
- Microfluïdische array-vangsten, houdt enkele cervicale cellen vast voor snellere screening

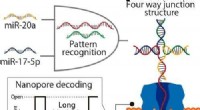
- Nanopore-technologie met DNA-computing detecteert gemakkelijk microRNA-patronen van longkanker
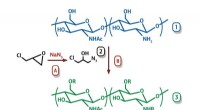
- Chemici verkrijgen nieuw materiaal voor antibacteriële voedselcoatings
- Met een keukenvriezer en plantaardige cellulose, een aerogel voor therapeutisch gebruik is ontwikkeld

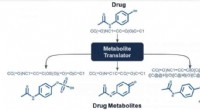
- Deep learning geeft medicijnontwerp een boost
 Onderzoek onthult nieuwe kwantumtoestand in vreemde isolatiematerialen
Onderzoek onthult nieuwe kwantumtoestand in vreemde isolatiematerialen Nieuwe techniek om de bevolking te berekenen in landen met volkstellingsproblemen
Nieuwe techniek om de bevolking te berekenen in landen met volkstellingsproblemen Wat is het aantal elektronen van het buitenste niveau voor eerste 18 elementen?
Wat is het aantal elektronen van het buitenste niveau voor eerste 18 elementen?  Waarom wordt natriumsulfiet gebruikt om permanganaatvlekken te verwijderen?
Waarom wordt natriumsulfiet gebruikt om permanganaatvlekken te verwijderen?  Wat is de juiste volgorde van de lagen van de atmosfeer, te beginnen met de laag die het dichtst bij de aarde ligt?
Wat is de juiste volgorde van de lagen van de atmosfeer, te beginnen met de laag die het dichtst bij de aarde ligt?  Welke planeet geeft meer energie dan het ontvangt van de zon?
Welke planeet geeft meer energie dan het ontvangt van de zon?  Als u 240 g suiker 50 ml kokend water toevoegt, wat zal de oplossing zijn?
Als u 240 g suiker 50 ml kokend water toevoegt, wat zal de oplossing zijn?  Chocolade uitgepakt - wat zit er in je paastraktatie?
Chocolade uitgepakt - wat zit er in je paastraktatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

