
Wetenschap
Wat is het aantal elektronen van het buitenste niveau voor eerste 18 elementen?
| Element | Symbool | Atomisch nummer | Valentie -elektronen |
| --- | --- | --- | --- |
| Waterstof | H | 1 | 1 |
| Helium | Hij | 2 | 2 |
| Lithium | Li | 3 | 1 |
| Beryllium | Zijn | 4 | 2 |
| Boron | B | 5 | 3 |
| Carbon | C | 6 | 4 |
| Stikstof | N | 7 | 5 |
| Zuurstof | O | 8 | 6 |
| Fluorine | F | 9 | 7 |
| Neon | NE | 10 | 8 |
| Natrium | NA | 11 | 1 |
| Magnesium | Mg | 12 | 2 |
| Aluminium | Al | 13 | 3 |
| Silicium | SI | 14 | 4 |
| Phosporus | P | 15 | 5 |
| Zwavel | S | 16 | 6 |
| Chloor | CL | 17 | 7 |
| Argon | AR | 18 | 8 |
Sleutelpunten:
* valentie -elektronen: Dit zijn de elektronen in het buitenste energieniveau van een atoom. Zij zijn degenen die betrokken zijn bij chemische binding.
* Periodieke trends: Het aantal valentie -elektronen neemt in het algemeen toe naarmate u van links naar rechts over een periode (rij) in de periodiek systeem beweegt. Het nummer wordt aan het begin van elke nieuwe periode gereset op 1.
* Uitzonderingen: Sommige elementen, met name in de overgangsmetalen, hebben meer gecompliceerde elektronenconfiguraties en hun valentie -elektronentelling volgen mogelijk dit eenvoudige patroon mogelijk niet.
Laat het me weten als je nog andere vragen hebt!
 Wat is de formule voor strontium gecombineerd met barium?
Wat is de formule voor strontium gecombineerd met barium?  Hoe de geleidbaarheid te berekenen vanwege concentratie
Hoe de geleidbaarheid te berekenen vanwege concentratie Wat is het aantal atomen elk element in zwaveldioxide?
Wat is het aantal atomen elk element in zwaveldioxide?  Mangaandioxide toont potentieel in micromotoren
Mangaandioxide toont potentieel in micromotoren Waarom vormt water waterstofbruggen?
Waarom vormt water waterstofbruggen?
Er zijn twee verschillende chemische bindingen aanwezig in water. De covalente bindingen tussen de zuurstof en de waterstofatomen zijn het gevolg van het delen van de elektronen. Dit is wat de watermoleculen zel
Hoofdlijnen
- Waarom vertrouwen spiercellen gewoonlijk op aërobe ademhaling in plaats van op fermentatie?
- Welke plantcel heeft een muur?
- Stimuleer stereotypen consumentenaankopen bij organisaties met of zonder winstoogmerk?
- Is het cytoplasma samengesteld uit cytoskelet?
- Hoe is de concentratie van een oplossing van invloed op osmose?
- Welk voordeel zou een organisme hebben als het bepaalde genen zou kunnen in- of uitschakelen als reactie op bepaalde omstandigheden?
- Hoe markergenen in celclusters te vinden
- Een evolutiepatroon waarin iets verschillende soorten evolueren van één gemeenschappelijke voorouder?
- Uit onderzoek blijkt hoe een tekort aan fosfor de accumulatie van anthocyanine in planten veroorzaakt
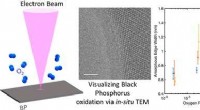
- Ingenieurs bevorderen inzichten over zwarte fosfor als materiaal voor toekomstige flexibele elektronica met ultralaag vermogen
- De mooiste zonnecellen zijn geïnspireerd door de natuur

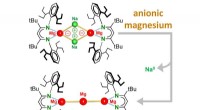
- Onderzoekers rapporteren omgekeerde magnesiumchemie-ontdekking
- De energie-implicaties van organische radicaalpolymeren

- Gebruikersexperiment bij BESSY II:complexe mozaïekpatronen, buitengewone materialen

 Wat was de primaire richting van de islamitische expansie van het Arabische schiereiland?
Wat was de primaire richting van de islamitische expansie van het Arabische schiereiland?  Stikstofonderzoek laat zien hoe sommige planten binnendringen en andere overnemen
Stikstofonderzoek laat zien hoe sommige planten binnendringen en andere overnemen  FRIPON-camera bovenop ESTEC
FRIPON-camera bovenop ESTEC Nintendo zegt samen te werken met Tencent om Switch in China uit te brengen
Nintendo zegt samen te werken met Tencent om Switch in China uit te brengen Geweldscriminaliteit neemt toe bij warmer weer, ongeacht het seizoen, studie vondsten
Geweldscriminaliteit neemt toe bij warmer weer, ongeacht het seizoen, studie vondsten Beschrijf de delen van bloemen
Beschrijf de delen van bloemen Voordelen van netvormende omvormers toegepast op fotovoltaïsche zonne-energiesystemen
Voordelen van netvormende omvormers toegepast op fotovoltaïsche zonne-energiesystemen Onbeleefde Uber-rijders kunnen worden opgestart vanuit de app
Onbeleefde Uber-rijders kunnen worden opgestart vanuit de app
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

