
Wetenschap
Oplossing van water en aspirine een zuur?
* aspirine (acetylsalicylzuur) is een zuur. Het heeft een carboxylgroep (-cooh) die een proton (H+) in oplossing kan doneren.
* Water is een zeer zwak zuur en een zeer zwakke basis. Het kan zowel een zuur als een basis werken, afhankelijk van de situatie.
* Wanneer aspirine in water wordt opgelost, doneert dit sommige van zijn protonen aan watermoleculen. Dit creëert hydroniumionen (H3O+) en het aspirinemolecuul wordt negatief geladen (aspirine -anion).
Dus de oplossing van water en aspirine is zuur. De aanwezige hydroniumionen maken de oplossing een pH lager dan 7.
Hier is een vereenvoudigde manier om erover na te denken:
* Aspirine geeft zijn protonen op (H+), waardoor de oplossing zuurder wordt.
* Water accepteert sommige van die protonen, maar het verandert de algehele zuurgraad niet erg.
Laat het me weten als je meer details wilt over de betrokken chemische reactie!
Hoofdlijnen
- Wat is een shereoid?
- Wat zijn scavenger carnivoren?
- Wanneer zijn in de celcyclus organellen gedupliceerd?
- Wat zijn het gebruik van de wetenschap in het echte leven?
- Sour Patch-volwassenen:1 op de 8 volwassenen houdt van extreme zuurheid, blijkt uit onderzoek
- Kunnen klonale planten eeuwig leven?
- Wat doet chloroplasten in je lichaam?
- Is het celmembraan bestaande uit cellen en waarom?
- Waar komt water uit het metabolisme vandaan?
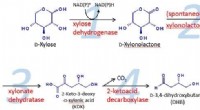
- Metabolic engineering methode slaagt erin om 1, 2, 4-butaantriol duurzaam uit biomassa
- Elektronen versterken de calorische koeling in vaste toestand in hexagonale sulfiden

- Gehyperpolariseerde proton-MRI gebruikt om metabolische processen in realtime te observeren

- Diagnose van kunstacne in Georgia OKeeffes-schilderijen

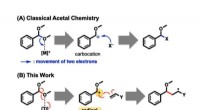
- Radicale chemie maakt eenvoudige synthese van ethers mogelijk
 Wat is een astrophy -Issist?
Wat is een astrophy -Issist?  Russische hongersnood van 1891
Russische hongersnood van 1891 Wat zijn de 3 basisstructuren die een bodem kan hebben?
Wat zijn de 3 basisstructuren die een bodem kan hebben?  Hoe kan de maan elektriciteit opwekken?
Hoe kan de maan elektriciteit opwekken?  Wat betekent geografisch rooster?
Wat betekent geografisch rooster?  Wat is een sterk zuur NaOH HF NH3 HCl?
Wat is een sterk zuur NaOH HF NH3 HCl?  Hoe zeewier wetenschappers heeft misleid over de gezondheid van riffen
Hoe zeewier wetenschappers heeft misleid over de gezondheid van riffen  Libellen laten zien hoe de biodiversiteit verandert in tijd en ruimte
Libellen laten zien hoe de biodiversiteit verandert in tijd en ruimte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


