
Wetenschap
Wat is de meest voorkomende lading van elementen voor fosfor?
De meest voorkomende lading van elementen voor fosfor is -3 .
Dit is waarom:
* Elektronenconfiguratie: Fosfor heeft 5 elektronen in zijn buitenste schaal. Om een stabiel octet te bereiken, heeft het de neiging om 3 elektronen te krijgen.
* Vorming van anionen: Het verkrijgen van 3 elektronen resulteert in een fosforion met een lading van -3 (p³⁻).
* Gemeenschappelijke verbindingen: Fosfor vormt vele verbindingen met deze -3 lading, zoals fosfaten (po₄³⁻) gevonden in meststoffen en DNA.
Hoewel fosfor soms andere ladingen kan hebben, zoals +5 in sommige verbindingen, is -3 de meest voorkomende en stabiele oxidatietoestand.
 Wat zijn de drie basisstaten van materiaal?
Wat zijn de drie basisstaten van materiaal?  Wat is de standaard molaire vormingsenthalpie voor ammoniumchloride aq?
Wat is de standaard molaire vormingsenthalpie voor ammoniumchloride aq?  Fujitsu ontwikkelt technologie om biochemische reacties te voorspellen, opheldering van de mechanismen van genetische aandoeningen
Fujitsu ontwikkelt technologie om biochemische reacties te voorspellen, opheldering van de mechanismen van genetische aandoeningen Tafelzout is het resultaat van?
Tafelzout is het resultaat van?  Insecten in vriesgebieden hebben een eiwit dat werkt als antivries
Insecten in vriesgebieden hebben een eiwit dat werkt als antivries
 Zuid-Amerikaanse vulkaan vertoont vroege waarschuwingssignalen van mogelijke instorting, uit onderzoek blijkt
Zuid-Amerikaanse vulkaan vertoont vroege waarschuwingssignalen van mogelijke instorting, uit onderzoek blijkt Ontdekkingsreizigers onderzoeken het verzonken continent Zeelandia
Ontdekkingsreizigers onderzoeken het verzonken continent Zeelandia Waardoor is de zwaartekracht ontstaan en hoe beïnvloedt deze het universum?
Waardoor is de zwaartekracht ontstaan en hoe beïnvloedt deze het universum?  Geen nadelige effecten van grazend vee op gewasresten:onderzoek in Nebraska
Geen nadelige effecten van grazend vee op gewasresten:onderzoek in Nebraska Opwarmende zeeën kunnen de frequentie van extreme stormen verhogen
Opwarmende zeeën kunnen de frequentie van extreme stormen verhogen
Hoofdlijnen
- Hoe het menselijk geheugen werkt
- Wat wordt bedoeld met L in een wetenschappelijke of botanische naam?
- Onderzoekstopics in Biotechnology
- Naarmate het klimaat warmer wordt, meer vogelnesten worden vernietigd in Finse landbouwgronden
- Wat beoordelen wetenschapper voordat hij hypothesen vormt?
- Uitvindingen van de evolutie:wat kikkers een gezicht geeft
- Het ochtendkoor horen:Okina was een nieuw akoestisch monitoringnetwerk
- Hoe is een meer of rivier die over de organismen in water wordt bevriest?
- Zijn dubbelgangers echt? Er is een kans van 1 op een biljoen
- De opmerkelijke variabiliteit van elektronische structuren van actinidetetrafluoride

- Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen

- Onderzoekers realiseren 4D-geprint materiaal

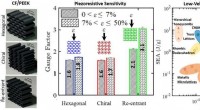
- lichtgewicht, slagvaste honingraatstructuren kunnen voelen wanneer ze beschadigd zijn
- Nieuw promiscue enzym helpt plantenafval om te zetten in duurzame producten

 Wanneer u de gaten in een sintelblok vult, welke kant is boven?
Wanneer u de gaten in een sintelblok vult, welke kant is boven?  Hoe muizenembryo's links van rechts bepalen
Hoe muizenembryo's links van rechts bepalen  Wat bedoel je met ferro en non-ferro?
Wat bedoel je met ferro en non-ferro?  Stortplaats omzetten in energie
Stortplaats omzetten in energie Waarom Augusts Moon bekend staat als de Sturgeon Moon
Waarom Augusts Moon bekend staat als de Sturgeon Moon  Bereken elektronenconfiguratie
Bereken elektronenconfiguratie Wat is de functie van cytoplasma in een cel?
Wat is de functie van cytoplasma in een cel?  Laserboor zet een nieuw wereldrecord in lasergestuurde elektronenversnelling
Laserboor zet een nieuw wereldrecord in lasergestuurde elektronenversnelling
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

