
Wetenschap
Waarom is benzine ontvlambaar en water niet, hoewel niet beide vloeistoffen zijn?
benzine (benzine):
* Samenstelling: Benzine is een complex mengsel van koolwaterstoffen, voornamelijk alkanen met variërende koolstofketenlengtes.
* Moleculaire structuur: Koolwaterstoffen hebben een hoog aandeel koolstof- en waterstofatomen, die sterke bindingen vormen. Deze bindingen worden gemakkelijk verbroken door warmte, waardoor energie wordt vrijgelaten en zeer reactieve moleculen vormen.
* Vijnbaarheid: De aanwezigheid van veel koolstofhydrogen bindingen maakt benzine gemakkelijk brandbaar. De hitte van een vonk of vlam biedt de energie om deze bindingen te verbreken, waardoor een kettingreactie wordt geïnitieerd die meer warmte vrijgeeft en snel vuur verspreidt.
Water:
* Samenstelling: Water is een eenvoudig molecuul dat bestaat uit twee waterstofatomen en één zuurstofatoom (H2O).
* Moleculaire structuur: Het zuurstofatoom vormt sterke polaire covalente bindingen met de waterstofatomen. Deze polaire structuur resulteert in waterstofbinding, waardoor water een zeer stabiel molecuul maakt.
* Niet-vluchtbaarheid: Water is niet ontvlambaar omdat de sterke bindingen tussen waterstof- en zuurstofatomen een aanzienlijke hoeveelheid energie vereisen om te breken. Deze energie is niet direct verkrijgbaar bij een eenvoudige vonk of vlam. Bovendien zijn watermoleculen zeer resistent tegen oxidatie (brandend) en remmen het verbrandingsproces actief.
Sleutelverschil: Het belangrijkste verschil ligt in de chemische bindingssterkte en moleculaire structuur . Benzine, met zijn overvloed aan zwakkere koolstofhydrogene bindingen, geeft gemakkelijk energie vrij en vormt reactieve moleculen bij blootstelling aan warmte, waardoor het brandbaar is. Water, met zijn sterke polaire bindingen en stabiele structuur, vereist veel meer energie om af te breken en is niet gemakkelijk brandbaar.
Samenvattend: De chemische samenstelling en moleculaire structuur van Petrol maken het zeer brandbaar, terwijl de unieke structuur en sterke bindingen van het water het niet-ontspannend maken.
 Op koolstof gebaseerde benaderingen voor het redden van regenwouden moeten biodiversiteitsstudies omvatten
Op koolstof gebaseerde benaderingen voor het redden van regenwouden moeten biodiversiteitsstudies omvatten Welke planten zullen groeien onder de rivier de berken?
Welke planten zullen groeien onder de rivier de berken?  Lijst met eencellige organismen
Lijst met eencellige organismen  Pacific Ocean maakt plaats voor 's werelds volgende supercontinent
Pacific Ocean maakt plaats voor 's werelds volgende supercontinent Studie:Noordwest hittegolf onmogelijk zonder klimaatverandering
Studie:Noordwest hittegolf onmogelijk zonder klimaatverandering
Hoofdlijnen
- Hoe jasmonaatsignalering wordt verbeterd onder fosforarme omstandigheden in de plantenfysiologie
- Welke klassen van biologische macromoleculen waartoe enzymen en zetmeel behoren?
- Wat is de functie van celmambraan?
- Deoxygenatie van de oceaan:een stille aanjager van de ondergang van koraalriffen?
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Hoeveel cellen hebben levende wezens?
- Wat zijn de twee belangrijkste toepassingen van ATP?
- Op welke manieren kunnen bacteriën bijdragen aan het succes van een tuin waarin erwtplanten groeien?
- Hoe wilskracht werkt
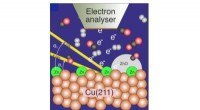
- Onderzoekers ontrafelen de actieve fase in katalytische reductie van kooldioxide tot methanol
- Eenden bieden onderzoekers een unieke kans om menselijke aanraking te bestuderen
- Nieuwe meettechniek kan pulpfabrieken miljoenen besparen

- 3D-printen en maanstof:een astronautenkit voor toekomstige ruimteverkenning?

- Onderzoekers ontwikkelen nieuwe methoden om microfluïdische apparaten te maken met fluorpolymeren

 In welke kleur zou koolstofdioxide kalkwater veranderen?
In welke kleur zou koolstofdioxide kalkwater veranderen?  'S Werelds eerste grafeenproduct met 3D-strutted-structuur
'S Werelds eerste grafeenproduct met 3D-strutted-structuur Heb jij de juiste persoonlijkheid voor Facebook?
Heb jij de juiste persoonlijkheid voor Facebook? Welk continent is 210 graden lengtegraadlijn in Antarctica?
Welk continent is 210 graden lengtegraadlijn in Antarctica?  AI gebruiken om een laser te richten om kakkerlakken te doden
AI gebruiken om een laser te richten om kakkerlakken te doden Is silicium vergelijkbaar met een niet-metaal?
Is silicium vergelijkbaar met een niet-metaal?  China prijst technische hoogstandjes van nieuwe internationale luchthaven
China prijst technische hoogstandjes van nieuwe internationale luchthaven Onderzoekers onderzoeken hoe een koolstoffixerend organel ontstaat via fasescheiding
Onderzoekers onderzoeken hoe een koolstoffixerend organel ontstaat via fasescheiding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

