
Wetenschap
Hoe identificeer je of een stof metalen matalloïde of niet -metaal is?
1. Metalen
* Fysieke eigenschappen:
* glanzend: De meeste metalen hebben een glanzend, reflecterend oppervlak.
* kneedbaar: Ze kunnen in dunne vellen worden gehamerd.
* ductiel: Ze kunnen in draden worden getrokken.
* Goede dirigenten: Ze voeren warmte en elektriciteit goed.
* vast bij kamertemperatuur: (Behalve voor kwik, wat vloeibaar is)
* Hoge dichtheid: Metalen zijn over het algemeen dicht.
* chemische eigenschappen:
* Vormen kationen: Ze hebben de neiging elektronen te verliezen en positief geladen ionen (kationen) te vormen.
* reactief: Sommige metalen zijn zeer reactief (zoals natrium en kalium), terwijl andere minder reactief zijn (zoals goud en platina).
2. Niet -metalen
* Fysieke eigenschappen:
* saai: Niet -metalen missen een glanzend uiterlijk.
* bros: Ze hebben de neiging gemakkelijk te breken.
* slechte geleiders: Het zijn slechte geleiders van warmte en elektriciteit (behalve koolstof in de vorm van grafiet).
* gassen bij kamertemperatuur: Veel niet -metalen zijn gassen bij kamertemperatuur (zuurstof, stikstof, chloor).
* Lage dichtheid: Niet -metalen zijn over het algemeen minder dicht dan metalen.
* chemische eigenschappen:
* Vorm anionen: Ze hebben de neiging elektronen te krijgen en negatief geladen ionen (anionen) te vormen.
* gevarieerde reactiviteit: Niet -metalen vertonen een breed scala aan reactiviteit.
3. Metalloïden (semimetalen)
* eigenschappen: Metalloïden hebben eigenschappen die ergens tussen metalen en niet -metalen vallen.
* halfgeleiders: Ze leiden elektriciteit beter dan niet -metalen, maar niet zo goed als metalen. Hun geleidbaarheid kan worden gecontroleerd, waardoor ze waardevol zijn in elektronica.
* bros: Metalloïden zijn over het algemeen bros.
* glanzend of saai: Hun uiterlijk kan variëren.
* vast bij kamertemperatuur: Metalloïden zijn vast bij kamertemperatuur.
Voorbeelden:
* metalen: IJzer (Fe), koper (Cu), goud (au), aluminium (AL), zilver (Ag)
* niet -metalen: Zuurstof (O), stikstof (N), chloor (CL), zwavel (s), fosfor (p), broom (br)
* metalloïden: Silicium (SI), Germanium (GE), Arseen (As), Antimony (SB), Tellurium (TE)
Sleutelpunt: Hoewel deze eigenschappen nuttig zijn voor het identificeren van metalen, niet -metalen en metalloïden, zijn er uitzonderingen op elke regel. Raadpleeg altijd naar een periodieke tabel ter bevestiging.
 Uitgebreide modellering van waterbronnen toegankelijker maken
Uitgebreide modellering van waterbronnen toegankelijker maken Miniatuurtranspondertechnologie voor gebruik in de strijd tegen plastic in de oceaan
Miniatuurtranspondertechnologie voor gebruik in de strijd tegen plastic in de oceaan Wat veroorzaakt neiging?
Wat veroorzaakt neiging?  Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat
Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat  Wetenschap zegt:tijdperk van monsterlijke orkanen die de Atlantische Oceaan bestormen
Wetenschap zegt:tijdperk van monsterlijke orkanen die de Atlantische Oceaan bestormen
Hoofdlijnen
- Wat zijn enkele geërfde eigenschappen van planten en dieren die in het grasland wonen?
- Welke organel bepaalt de structurele en functionele kenmerken van cellen door het regelen van RNA -eiwitsynthese?
- Wat is een voorbeeld van bioremediatie?
- Australische soorten hebben een onafhankelijke kampioen nodig
- Babymanta's:nieuw licht op hun leven in Indonesische waterspeeltuin
- Welke ziekten worden veroorzaakt door spiraalvormige bacteriën?
- Welke soort heeft bij pH 7,5 de overhand op H3PO4?
- Hoe reproduceert Ascomycota zich?
- Welke monosacharide is een bouwsteen van de muur van de plantencel?
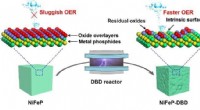
- Etsproces verbetert de extractie van waterstof tijdens elektrolyse van water
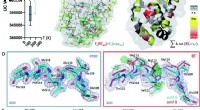
- Het vergelijken van cryogene structuren met monsters op kamertemperatuur kan helpen bij het identificeren van fouten in rekenmodellen
- Vloeistofachtige beweging in kristallen zou hun veelbelovende gedrag in zonnecellen kunnen verklaren

- Licht van zeldzame aarde:nieuwe kansen voor organische light-emitting diodes
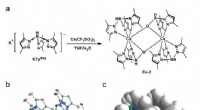
- Synthetische fysiologen ontwikkelen nieuwe receptor uitgeschakeld door groen licht

 Hoe veranderen de isolerende eigenschappen van een jas als het isolatiemateriaal nat wordt?
Hoe veranderen de isolerende eigenschappen van een jas als het isolatiemateriaal nat wordt?  Wat zorgt ervoor dat sterren er kleiner uitzien dan ze werkelijk zijn?
Wat zorgt ervoor dat sterren er kleiner uitzien dan ze werkelijk zijn?  Wat is de ergste uitbarsting van Santorini Volcano in Griekenland?
Wat is de ergste uitbarsting van Santorini Volcano in Griekenland?  Onderzoekers ontdekken wat pneumokokken je ziek maken
Onderzoekers ontdekken wat pneumokokken je ziek maken  Hoe plasmaconverters werken
Hoe plasmaconverters werken  Nieuwe glucagon-achtige peptide-1 medicijnen ontworpen voor diabetes type 2
Nieuwe glucagon-achtige peptide-1 medicijnen ontworpen voor diabetes type 2 Nieuwe afbraakeiwitten tonen de route naar celoverleving
Nieuwe afbraakeiwitten tonen de route naar celoverleving  Hoe een nieuwe warmtebatterij miljoenen huizen snel gasloos kan maken
Hoe een nieuwe warmtebatterij miljoenen huizen snel gasloos kan maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

