
Wetenschap
Waarom zal een alkalimetaal vaak combineren met een halogeen nonmetal om samenstelling te vormen?
Hier is een uitsplitsing:
* Alkali -metalen: Hebben één valentie -elektron (elektron in de buitenste schaal) en een sterke neiging om te verliezen Dit elektron om een stabiel octet te bereiken (acht elektronen in de buitenste schaal). Dit verlies maakt hen positief geladen ionen (kationen).
* halogenen: Hebben zeven valentie -elektronen en een sterke neiging tot winst Eén elektron om een stabiel octet te bereiken. Deze winst maakt ze negatief geladen ionen (anionen).
Wanneer een alkalimetaal en een halogeen elkaar ontmoeten, geeft het alkalimetaal gemakkelijk zijn valentie -elektron aan het halogeen, waardoor een stabiele ionische binding wordt gevormd vanwege de sterke elektrostatische aantrekkingskracht tussen de tegengesteld geladen ionen.
Voorbeeld: Natrium (NA) en chloor (CL) reageren op natriumchloride (NaCl).
* Natrium (NA) verliest één elektron om een positief geladen natriumion (Na+) te worden.
* Chloor (CL) krijgt één elektron als een negatief geladen chloride-ion (Cl-).
* De tegengesteld geladen ionen trekken elkaar sterk aan en vormen een stabiel verbinding, natriumchloride (NaCl).
Dit proces staat ook bekend als ionische binding , wat een belangrijke drijvende kracht is achter de vorming van verbindingen tussen alkali -metalen en halogenen.
 Het Atlantische orkaanseizoen zou een recordbreker kunnen zijn
Het Atlantische orkaanseizoen zou een recordbreker kunnen zijn  Afbeelding:berg Fuji, Japan
Afbeelding:berg Fuji, Japan Ambtenaren zetten zich schrap voor onzekerheid over de wateroverdrachten naar Lake Mead
Ambtenaren zetten zich schrap voor onzekerheid over de wateroverdrachten naar Lake Mead  Onderzoek toont potentieel schadelijke arseenniveaus aan bij populaire voormalige mijnbouwwerken
Onderzoek toont potentieel schadelijke arseenniveaus aan bij populaire voormalige mijnbouwwerken Ozark graslanden ervaren grote toename van bomen en struiken
Ozark graslanden ervaren grote toename van bomen en struiken
Hoofdlijnen
- Misplaatste monarchen:clusters van vlinders in het noorden
- Gluconeogenese beschrijft de conversie van wat?
- Waarom zijn decomposers essentieel voor de creatie?
- Lariats:Hoe beslissingen over RNA-splitsing worden genomen
- Hoe polyfasische slaap werkt
- Wat wordt er geproduceerd wanneer eiwit vooraf wordt verdeeld?
- Inzicht in hoe cellen reageren op fysieke signalen zou tot nieuwe ziektebehandelingen kunnen leiden
- Indringende vraag:Moet de samenleving reproductieve technologieën reguleren?
- Wat is de functie van borstelreiniger in het laboratorium?
- Onderzoekers patenteren snelle tests voor cocaïne

- Onderzoekers ontwikkelen de eerste functionele niet-eigen metaalhydrogenase

- Ingenieurs evalueren de factoren die de batterijprestaties bij lage temperaturen beïnvloeden

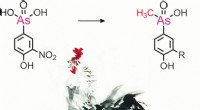
- Gemethyleerde fenylarsenische metabolieten geïdentificeerd in kippenlevers
- Een proefschrift bracht nieuwe hi-precisie massametingen voor atomaire massa's van isotopen zwaarder dan ijzer

 We maken neppoep in een laboratorium – om de sanitaire voorzieningen in Bangladesh te verbeteren
We maken neppoep in een laboratorium – om de sanitaire voorzieningen in Bangladesh te verbeteren Nieuw warmtemodel kan ervoor zorgen dat elektronische apparaten langer meegaan
Nieuw warmtemodel kan ervoor zorgen dat elektronische apparaten langer meegaan Welk metaal verliest het gemakkelijkst elektronen natrium of kalium?
Welk metaal verliest het gemakkelijkst elektronen natrium of kalium?  Wat houdt ons tegen om algen en anaërobe bacteriën naar Mars te lanceren om te beginnen met terravorming voor mogelijke toekomstige bewoning?
Wat houdt ons tegen om algen en anaërobe bacteriën naar Mars te lanceren om te beginnen met terravorming voor mogelijke toekomstige bewoning?  Heeft Saturnus unieke kenmerken?
Heeft Saturnus unieke kenmerken?  ECB lanceert realtime betalingen als uitdaging voor techreuzen
ECB lanceert realtime betalingen als uitdaging voor techreuzen Hoe maakt piëzo-elektrische energie elektriciteit?
Hoe maakt piëzo-elektrische energie elektriciteit?  Beschrijf in het algemeen de structuur- en interieurdichtheidsdruktemperatuuromstandigheden van een gemiddelde ster zoals zon?
Beschrijf in het algemeen de structuur- en interieurdichtheidsdruktemperatuuromstandigheden van een gemiddelde ster zoals zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

