
Wetenschap
Wat zijn de vier mechanismen die substraten krijgen naar de overgangstoestand?
1. Nabijheid en oriëntatie: Enzymen brengen reactanten samen in de juiste oriëntatie om de reactie te vergemakkelijken. Dit vermindert de entropie van het systeem, waardoor de reactie gunstiger wordt.
2. Zeef of vervorming: Enzymen kunnen substraten binden op een manier die hun vorm vervormt, waardoor ze reactiever worden. Dit wordt vaak bereikt door bindende substraten in een conformatie dicht bij de overgangstoestand.
3. Elektrostatische interacties: Enzymen kunnen geladen aminozuren of cofactoren gebruiken om de overgangstoestand te stabiliseren en de energie te verlagen. Dit is vooral belangrijk voor reacties met geladen gemiddelden.
4. Katalyse van zure base: Enzymen kunnen aminozuurresiduen gebruiken om protonen te doneren of te accepteren, waardoor de vorming van de overgangstoestand wordt vergemakkelijkt. Dit is cruciaal voor reacties met protonenoverdracht.
Andere belangrijke mechanismen:
* Katalyse van metaalionen: Sommige enzymen gebruiken metaalionen om geladen tussenproducten te stabiliseren of om redoxreacties te vergemakkelijken.
* Covalente katalyse: Enzymen kunnen tijdelijke covalente bindingen vormen met substraten om hun reactiviteit te veranderen.
Het is belangrijk om te onthouden dat deze mechanismen vaak samenwerken in een complex samenspel om het gewenste katalytische effect te bereiken. Het specifieke mechanisme hangt af van het individuele enzym en de reactie die worden gekatalyseerd.
 Team demonstreert grote belofte van volledig anorganische perovskiet-zonnecellen voor het verbeteren van de efficiëntie van zonnecellen
Team demonstreert grote belofte van volledig anorganische perovskiet-zonnecellen voor het verbeteren van de efficiëntie van zonnecellen Team maakt allereerste VX-neurotoxinedetector
Team maakt allereerste VX-neurotoxinedetector Wat is de bron van koolstof voor ademhaling?
Wat is de bron van koolstof voor ademhaling?  Bij de reactie van een zuur met een base ontstaat zout. Wat is het andere product?
Bij de reactie van een zuur met een base ontstaat zout. Wat is het andere product?  Wat betekent de term in chemie?
Wat betekent de term in chemie?
 Op zoek naar de sleutel om 20 dagen van tevoren hittegolven boven het stroomgebied van de Yangtze-rivier te voorspellen
Op zoek naar de sleutel om 20 dagen van tevoren hittegolven boven het stroomgebied van de Yangtze-rivier te voorspellen Naarmate de kolenindustrie krimpt, mijnwerkers verdienen een rechtvaardige transitie - dit moet het bevatten
Naarmate de kolenindustrie krimpt, mijnwerkers verdienen een rechtvaardige transitie - dit moet het bevatten Klein maar krachtig:waarom microben deel kunnen uitmaken van klimaatoplossingen
Klein maar krachtig:waarom microben deel kunnen uitmaken van klimaatoplossingen  Australië moet stoppen met het bouwen van huizen in dergelijke brandgevoelige gebieden
Australië moet stoppen met het bouwen van huizen in dergelijke brandgevoelige gebieden Blikseminslagen kunnen op korte termijn dunner worden in de ozonlaag
Blikseminslagen kunnen op korte termijn dunner worden in de ozonlaag
Hoofdlijnen
- Wat betekent rol in wetenschapstermen?
- Hoe cheeta's de windhonden overtreffen
- Wat zijn de secties van DNA die codeert voor een eiwit en de kern verlaten?
- Wat voor soort biome is Abbotsford?
- Nieuw onderzoek laat zien hoe amyloïde bèta de hersencellen binnendringt
- Wat is een ongeldige hypothese?
- Hormoonnabootsingen in plastic waterflessen – slechts het topje van de ijsberg?
- Het type organismen dat voedselergie door een gemeenschap overdragen en uiteindelijk eten met andere zijn de?
- Hoe wordt DNA genoemd tijdens celdeling?
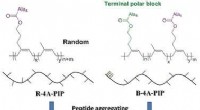
- Biomimetische strategie leidt tot sterke, recyclebaar rubber
- Database voor stegananalyse van forensisch bewijs

- Fout gevonden in waterbehandelingsmethode:het proces kan onbewust schadelijke chemicaliën genereren

- Superdiamond koolstof-borium kooien kunnen verschillende eigenschappen opvangen en aanboren

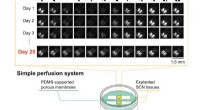
- Hersenweefsel wekenlang in leven gehouden op een kunstmatig membraan
 Hoe zijn de verdeeldheid tussen cellen in veel schimmels genaamd-?
Hoe zijn de verdeeldheid tussen cellen in veel schimmels genaamd-?  Computers en de zoektocht naar nieuwe planeten
Computers en de zoektocht naar nieuwe planeten Hoe wordt het de geordende volgorde van reacties genoemd die de opslagplaats verplaatsen en energie vrijgeven?
Hoe wordt het de geordende volgorde van reacties genoemd die de opslagplaats verplaatsen en energie vrijgeven?  Het lawaai van de menigte deconstrueren bij basketbalwedstrijden op de universiteit
Het lawaai van de menigte deconstrueren bij basketbalwedstrijden op de universiteit Zelfs machines hebben hun groenten nodig
Zelfs machines hebben hun groenten nodig Wat is het belang van evolutietheorie?
Wat is het belang van evolutietheorie?  Duurzame oplossingen met Zuid-Afrika in de strijd tegen waterschaarste
Duurzame oplossingen met Zuid-Afrika in de strijd tegen waterschaarste Waarom worden natte kleding op de draad verspreid om ze snel te drogen?
Waarom worden natte kleding op de draad verspreid om ze snel te drogen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

