
Wetenschap
Waarom oplost bariumsulfaat niet in HCL?
* Lage oplosbaarheid: Bariumsulfaat is inherent zeer slecht oplosbaar in water. Dit betekent dat het niet gemakkelijk uiteenvalt in zijn samenstellende ionen (ba
* stabiele vaste stof: Bariumsulfaat vormt een zeer stabiele vaste roosterstructuur. De sterke elektrostatische attracties tussen de bariumkationen (ba
* Geen reactie met HCl: Hoewel HCL een sterk zuur is, reageert het niet met bariumsulfaat om een oplosbare verbinding te vormen. De chloride-ionen (Cl
-
) Van HCl verplaatsen de sulfaationen niet gemakkelijk (dus 4
Belangrijke opmerking: Hoewel bariumsulfaat niet oplost in HCl, kan het worden opgelost in geconcentreerd zwavelzuur (H 2 Dus 4 ). Dit komt omdat de toevoeging van overtollige sulfaationen het evenwicht verschuift naar de vorming van meer oplosbaar bariumsulfaat, waardoor de vaste stof effectief oplost. Dit is echter een zeer gespecialiseerde reactie en wordt meestal niet gebruikt in dagelijkse scenario's.
Samenvattend maakt de combinatie van lage oplosbaarheid, stabiele vaste structuur en gebrek aan een reactie met HCL bariumsulfaat onoplosbaar in zoutzuur.
Hoofdlijnen
- Opinie:het wegen van in het laboratorium gekweekte biefstuk - de problemen met het eten van vlees zijn geen Silicon Valleys om op te lossen
- Wat is het wortelsysteem genoemd in een bryofyt?
- Wat gebeurt er tijdens meiose anafase 1?
- Waarom is transpiratie belangrijk in de watercyclus?
- Wat zijn biotische factoren bij varkens?
- Op diamanten gebaseerde kwantumdetectiemicroscoop biedt een effectieve aanpak voor het kwantificeren van cellulaire krachten
- Wat hebben alle levende organismen gemeen?
- Nieuwe details over hoe een viraal eiwit de replicatie van virussen remt
- Welke verklaring verklaart het beste de betekenis van meiose in procesevolutie binnen soorten?
- Het bedekken van metalen katalysatoroppervlakken met dunne tweedimensionale oxidematerialen kan chemische reacties versterken
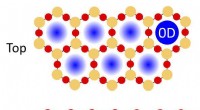
- Wetenschappers vinden nieuw sensing-oogmasker uit

- Koolwaterstoffen verteren

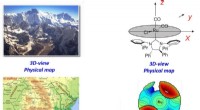
- Het in kaart brengen van de driedimensionale structuur van katalytische centra helpt bij het ontwerpen van nieuwe en verbeterde katalysatoren
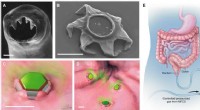
- Gastro-intestinaal-bewoner, vormveranderende microdevices voor verlengde medicijnafgifte
 Wie heeft de zonne -nevelhypothese uitgevonden?
Wie heeft de zonne -nevelhypothese uitgevonden?  Hoe biobrandstoffen uit plantaardige vezels de opwarming van de aarde kunnen tegengaan
Hoe biobrandstoffen uit plantaardige vezels de opwarming van de aarde kunnen tegengaan  Soorten microscopen en hun functies?
Soorten microscopen en hun functies?  Onderzoekers rapporteren MRI op atomaire schaal
Onderzoekers rapporteren MRI op atomaire schaal Hoe vlinders transparante vleugels maken:wetenschappers zien het onzichtbare
Hoe vlinders transparante vleugels maken:wetenschappers zien het onzichtbare  Sluit Nike zich aan bij de selectie van Amazon?
Sluit Nike zich aan bij de selectie van Amazon?  Elektriciteitsprijzen hebben recordhoogtes bereikt, en de tijd-armen zouden het meest kunnen lijden
Elektriciteitsprijzen hebben recordhoogtes bereikt, en de tijd-armen zouden het meest kunnen lijden Natuurkundigen grijpen individuele atomen in baanbrekend experiment
Natuurkundigen grijpen individuele atomen in baanbrekend experiment
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


