
Wetenschap
Een element dat een zeer reactief gas is, waarschijnlijk lid van het wat?
Een zeer reactief gas is hoogstwaarschijnlijk een lid van de halogeengroep .
Dit is waarom:
* halogenen bevinden zich in groep 17 van het periodieke tabel. Ze hebben 7 valentie -elektronen, waardoor ze zeer elektronegatief zijn en graag nog een elektron krijgen om een stabiel octet te bereiken.
* Dit sterke verlangen om een elektron te winnen maakt ze zeer reactief, vooral met metalen.
* Voorbeelden van halogenen zijn onder meer: Fluor (F), chloor (CL), bromine (BR), jodium (I) en astatine (AT). Dit zijn allemaal gassen bij kamertemperatuur behalve broom, wat een vloeistof is.
Laat het me weten als je meer wilt weten over de halogenen!
 Opwarming van de oceaan en verzuringseffecten op kalkhoudende fytoplanktongemeenschappen
Opwarming van de oceaan en verzuringseffecten op kalkhoudende fytoplanktongemeenschappen Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen
Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen Uit onderzoek blijkt dat het jaarlijkse risico van extreme regenval in Texas zal stijgen van 1 naar 18 procent
Uit onderzoek blijkt dat het jaarlijkse risico van extreme regenval in Texas zal stijgen van 1 naar 18 procent Afbeelding:Wildvuurvonken in suikerrietvelden op het eiland Maui
Afbeelding:Wildvuurvonken in suikerrietvelden op het eiland Maui Wat is het land voor Beryllium?
Wat is het land voor Beryllium?
Hoofdlijnen
- Natuurbeschermers bevestigen de vierde aanval van grijze wolven in Grand County in Colorado
- Stuctuur van een celmembraan
- Nieuw onderzoek wijst uit dat walvistanden na het midden van de dracht nog steeds aanwezig zijn, wat enigszins verrassend is
- Studie biedt een krachtige computermodelleringsbenadering voor celsimulaties
- In welk bioom werken ontleders het meest efficiënt?
- Begrepen lysosomen organellen die hun nut hebben overleefd?
- Onderzoekers detecteren signalen van parasieten in mest van amfibieën
- Waar is een variabele voor in wetenschappelijke experimenten?
- Ter verdediging van kamsalamanders - waarom deze ongrijpbare amfibieën de moeite waard zijn?
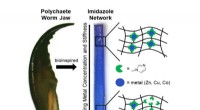
- Wetenschappers bootsen de dodelijke kaak van een worm na om veerkrachtige materialen te ontwerpen en te vormen
- Een 3D-aanpak om kanker te stoppen

- Onderzoekers produceren kosteneffectieve, milieuvriendelijk glasmateriaal

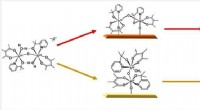
- Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is
- Comb breathalyzer is nu duizendmaal gevoeliger voor biomarkers voor ziekten

 Wereld om klimaatkeerpunt 2020 te missen:analyse
Wereld om klimaatkeerpunt 2020 te missen:analyse Wat zal eerst de Orion -ster of onze zon uitsterven?
Wat zal eerst de Orion -ster of onze zon uitsterven?  Hoe zeegezichten uit de oudheid de genetische structuur van Europese populaties hebben gevormd
Hoe zeegezichten uit de oudheid de genetische structuur van Europese populaties hebben gevormd Waarom bewegen de stofdeeltjes als een zonnestraal de kamer binnenkomt?
Waarom bewegen de stofdeeltjes als een zonnestraal de kamer binnenkomt?  Wat krijg je als je CH4 in O2 verbrandt?
Wat krijg je als je CH4 in O2 verbrandt?  Nieuwe kleurenfotografie met behulp van een zeer efficiënte sonde kan wit licht superfocussen op een punt van 6 nanometer
Nieuwe kleurenfotografie met behulp van een zeer efficiënte sonde kan wit licht superfocussen op een punt van 6 nanometer  Opzettelijk lesgeven heeft de grootste impact op de resultaten in de vroege kinderjaren
Opzettelijk lesgeven heeft de grootste impact op de resultaten in de vroege kinderjaren Wat bedoelde Einstein met energie niet gecreëerd of vernietigd alleen veranderd?
Wat bedoelde Einstein met energie niet gecreëerd of vernietigd alleen veranderd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

