
Wetenschap
Waarom is het moeilijker om de vorm van een vaste stof of vloeistof te veranderen?
* vaste stoffen: In vaste stoffen worden moleculen strak in elkaar verpakt en worden vastgehouden door sterke intermoleculaire krachten. Deze krachten zijn zo sterk dat de moleculen alleen op hun plaats kunnen trillen, waardoor vaste stoffen hun vaste vorm en volume hebben. Er is veel energie voor nodig om deze sterke krachten te overwinnen en de vorm van een vaste stof te veranderen. Zie het als proberen een baksteen te persen - het is heel moeilijk om van vorm te veranderen!
* vloeistoffen: Vloeistoffen hebben zwakkere intermoleculaire krachten dan vaste stoffen, waardoor de moleculen vrijer kunnen bewegen. Dit geeft vloeistoffen het vermogen om te stromen en de vorm van hun container te nemen, maar ze behouden nog steeds een relatief vast volume. De krachten zijn echter nog steeds sterk genoeg dat vloeistoffen weerstand bieden aan veranderingen in vorm, waardoor ze minder gemakkelijk vervormd zijn dan gassen. Denk aan het gieten van water in een glas - het neemt de vorm van het glas aan, maar het volume blijft hetzelfde.
* gassen: Gassen hebben de zwakste intermoleculaire krachten. Hun moleculen bewegen vrij rond en hebben geen vaste positie of volume. Daarom kunnen gassen gemakkelijk elke container vullen en gemakkelijk van vorm veranderen. Stel je voor dat je een ballon opblaast - de luchtmoleculen verspreiden zich en nemen de vorm van de ballon.
Samenvattend:
* Vaste stoffen zijn het moeilijkst om van vorm te veranderen vanwege hun sterke intermoleculaire krachten.
* Vloeistoffen zijn gemakkelijker vervormd dan vaste stoffen, maar weerstaan nog steeds vormveranderingen door zwakkere intermoleculaire krachten.
* Gassen zijn het gemakkelijkst om van vorm te veranderen omdat hun moleculen de zwakste intermoleculaire krachten hebben en vrij kunnen bewegen.
 New Yorks overdreven politieke benadering van openbaar vervoer
New Yorks overdreven politieke benadering van openbaar vervoer Hoe te vertellen of een eekhoorn mannelijk of vrouwelijk is
Hoe te vertellen of een eekhoorn mannelijk of vrouwelijk is De stikstofpuzzel oplossen:grondwaterverontreiniging door landbouw meten
De stikstofpuzzel oplossen:grondwaterverontreiniging door landbouw meten Low-flow-onderzoek op de Colorado-rivier werpt licht op het uiteindelijke nieuwe normaal voor Grand Canyon
Low-flow-onderzoek op de Colorado-rivier werpt licht op het uiteindelijke nieuwe normaal voor Grand Canyon Arctisch zee-ijsverlies intensiveert het transport van aerosolen naar het Tibetaanse plateau
Arctisch zee-ijsverlies intensiveert het transport van aerosolen naar het Tibetaanse plateau
Hoofdlijnen
- Wat doen microbiologen?
- Wiskundig model laat zien hoe een pitadder in het holst van de nacht zijn eten kan vinden
- Wat is de meest effectieve manier van metabolisme?
- Waarom is de hypothese zo belangrijk voor de wetenschappelijke methode?
- Waarom zijn gespecialiseerde cellen belangrijk voor multi-cellulaire organismen?
- Wat kun je concluderen over een eiwit met een hoog molecuulgewicht dat niet naar de kern kan worden getransporteerd?
- Wat maakt Bones moeilijk?
- Hebben dieren en planten DNA?
- Biologische activiteit kan de hoeveelheid van wat veranderen?
- Zelfs machines hebben hun groenten nodig

- Neutronenstudie van glaucoommedicijnen biedt aanwijzingen over enzymdoelen voor agressieve kankers

- Actieve camouflage kunsthuid in zichtbaar tot infrarood bereik

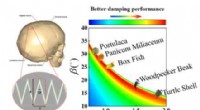
- De relatie tussen delicate hechtdraadstructuur en dempende prestaties van biomaterialen
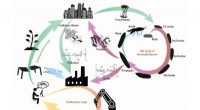
- Team ontwikkelt ontbrekende schakel naar circulaire economie en pakt wereldwijde verspilling aan
 Vraag en antwoord:Hoe het mensenrecht op een gezonde omgeving ons allemaal kan helpen beschermen
Vraag en antwoord:Hoe het mensenrecht op een gezonde omgeving ons allemaal kan helpen beschermen Wat zijn de primaire functies van fosfolipiden?
Wat zijn de primaire functies van fosfolipiden?  De nieuwe Star Wars zien? Wees voorzichtig met wat je wenst
De nieuwe Star Wars zien? Wees voorzichtig met wat je wenst Hoe verhoudt een sterrenstraal zich met hun massa?
Hoe verhoudt een sterrenstraal zich met hun massa?  Onderzoek onthult verrassend krachtige beet van kleine vroege tetrapod
Onderzoek onthult verrassend krachtige beet van kleine vroege tetrapod Wat doen de drie soorten RNA?
Wat doen de drie soorten RNA?  Onderzoekers onderzoeken een eigenaardige stervormende kandidaat voor een dwergstelsel
Onderzoekers onderzoeken een eigenaardige stervormende kandidaat voor een dwergstelsel Maak een lijst van drie belangrijkste deeltjes van een atoom en leg uit hoe ze van elkaar verschillen?
Maak een lijst van drie belangrijkste deeltjes van een atoom en leg uit hoe ze van elkaar verschillen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

