
Wetenschap
Heeft koolstof eigenschappen van metaal en niet -metalen?
Dit is waarom:
Niet-metaalachtige eigenschappen:
* Slechte warmtegeleider en elektriciteit: Koolstof in zijn meest voorkomende vormen (grafiet, diamant) is een slechte geleider van warmte en elektriciteit.
* bros: Koolstof is over het algemeen bros, wat betekent dat het gemakkelijk onder stress breekt.
* niet-heerlijk: Koolstof heeft niet het glanzende uiterlijk typisch voor metalen.
metaalachtige eigenschappen:
* kan legeringen vormen: Koolstof kan legeringen vormen met andere elementen, zoals in staal (ijzer met koolstof).
* kan ionische bindingen vormen: Koolstof kan ionische bindingen vormen met andere elementen, zoals bij carbonaten (CO3^2-).
* kan covalente netwerken vormen: Diamond, een vorm van zuivere koolstof, heeft een sterke covalente netwerkstructuur, die bijdraagt aan zijn hardheid en hoog smeltpunt.
Samenvatting:
De unieke combinatie van koolstof van metalen en niet -metalen eigenschappen maakt het een ongelooflijk veelzijdig element, dat in staat is om een breed scala aan verbindingen en materialen met verschillende eigenschappen te vormen. Het speelt cruciale rollen in het leven (organische moleculen), technologie (elektronica, materialen) en de structuur van de aarde (koolstofcyclus).
 Wat is de algemene vergelijking voor een zuur-base-reactie?
Wat is de algemene vergelijking voor een zuur-base-reactie?  Wat zijn dingen waar aan deeltjes in een vaste stof?
Wat zijn dingen waar aan deeltjes in een vaste stof?  Waarom is het belangrijk om het smelttraject van onzuivere en herkristalliseerde monsters vanilline te bepalen?
Waarom is het belangrijk om het smelttraject van onzuivere en herkristalliseerde monsters vanilline te bepalen?  Is cytoplasma vast, vloeibaar of gasvormig?
Is cytoplasma vast, vloeibaar of gasvormig?  De meeste eiwitinformatie ooit vastgelegd in een enkele cel dankzij nieuwe nanoPOTS-technologie
De meeste eiwitinformatie ooit vastgelegd in een enkele cel dankzij nieuwe nanoPOTS-technologie
 Schadelijke algenbloei kan in de lucht komen
Schadelijke algenbloei kan in de lucht komen Als consumenten plastic willen, maar ook zorgen maken over de planeet
Als consumenten plastic willen, maar ook zorgen maken over de planeet Voordelen van peulvruchten:goed voor u en de planeet
Voordelen van peulvruchten:goed voor u en de planeet Hoge economische en gezondheidskosten van luchtvervuiling door auto's in ontwikkelingslanden
Hoge economische en gezondheidskosten van luchtvervuiling door auto's in ontwikkelingslanden Hittegolven bedreigen stadsbewoners, vooral minderheden en de armen
Hittegolven bedreigen stadsbewoners, vooral minderheden en de armen
Hoofdlijnen
- Nieuwe irissoort ontdekt in de Langeberg Mountains, Zuid-Afrika
- Welke beschrijft het beste hoe ons begrip van DNA en erfelijke eigenschappen in de loop van de tijd is veranderd?
- Wat gebeurt er als twee verschillende soorten proberen dezelfde niche te bezetten?
- Hoe lang duurde het om een dinosaurusei uit te broeden? Onderzoek zegt 3-6 maanden
- Wat is de erfelijke ziekte van exocriene klieren die leidt tot luchtwegobstructie?
- Welke term wordt gedefinieerd als een lijst van elke nucleotidebasis voor soortenorganismen?
- Wanneer treedt melkzuurfermentatie op?
- Waarom gebruiken wetenschappers modellen van natuurlijke systemen die uw antwoord niet vertellen?
- Wat is het ultieme eindresultaat van glycolyse?
- Goedkoop, afdrukbaar 3D-apparaat ontworpen voor het analyseren van chemicaliën van smartphones

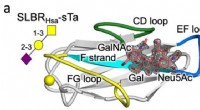
- Gebruikmaken van de structuur van bacteriële gastheercelreceptoren om kanker te detecteren
- Het mysterie openbreken hoeveel bubbels er in een glas bier zitten

- Universeel regulatiemechanisme in plantencellen ontdekt
- Upcycling van plastic zakken tot batterijonderdelen

 Welke ringde planeet met meerdere kleuren?
Welke ringde planeet met meerdere kleuren?  De microscopiemethode overwint de traditionele resolutielimiet voor het snel volgen van moleculen
De microscopiemethode overwint de traditionele resolutielimiet voor het snel volgen van moleculen  Discovery wijst de weg naar grafeencircuits
Discovery wijst de weg naar grafeencircuits Californische rook dreef in 2020 naar Europa en veroorzaakte zware vertroebeling van de zon
Californische rook dreef in 2020 naar Europa en veroorzaakte zware vertroebeling van de zon Waarom wordt zure regen geproduceerd?
Waarom wordt zure regen geproduceerd?  Wetenschappers vinden goedkopere manier om waterstof uit water te maken
Wetenschappers vinden goedkopere manier om waterstof uit water te maken Celstructuur van een dier
Celstructuur van een dier Wat zijn de overeenkomsten tussen sedimentaire rotsen van chemische oorsprong en die organische oorsprong?
Wat zijn de overeenkomsten tussen sedimentaire rotsen van chemische oorsprong en die organische oorsprong?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

