
Wetenschap
Wat mag bij het in evenwicht brengen van een chemische vergelijking zich aanpassen?
Dit is waarom:
* coëfficiënten vertegenwoordigen het aantal mol van elke reactant en product. Het veranderen van de coëfficiënt verandert het aantal moleculen of mol bij de reactie.
* subscripts in een chemische formule vertegenwoordigen het aantal atomen van elk element binnen een molecuul. U kan niet Verander de subscripts omdat dat de identiteit van de stof zelf zou veranderen.
Bijvoorbeeld:
Overweeg de onevenwichtige vergelijking:
`` `
H₂ + O₂ → H₂o
`` `
Om dit in evenwicht te brengen, passen we de coëfficiënten aan:
`` `
2h₂ + o₂ → 2h₂o
`` `
Verklaring:
* Initiële status: 2 waterstofatomen aan de linkerkant, 2 zuurstofatomen aan de linkerkant en 2 waterstofatomen en 1 zuurstofatoom aan de rechterkant.
* uitgebalanceerde status: 4 waterstofatomen en 2 zuurstofatomen aan beide zijden.
Door de coëfficiënten aan te passen, zorgen we ervoor dat het aantal atomen van elk element hetzelfde is aan beide zijden van de vergelijking, waardoor de wet van het behoud van massa wordt voldaan.
 Waar komt het aardgas dat wordt gebruikt in Bunsen -branders oorspronkelijk vandaan?
Waar komt het aardgas dat wordt gebruikt in Bunsen -branders oorspronkelijk vandaan?  Onderzoek onthult structuur van humane endogene reverse transcriptase
Onderzoek onthult structuur van humane endogene reverse transcriptase Nieuwe verfmethode kan jeans helpen het giftige probleem te verkleinen
Nieuwe verfmethode kan jeans helpen het giftige probleem te verkleinen  Wat zijn geen producten van een nucleaire splijtingsreactie?
Wat zijn geen producten van een nucleaire splijtingsreactie?  Wat is een voorbeeld van een gas tot vaste afzetting?
Wat is een voorbeeld van een gas tot vaste afzetting?
 Mensen ontsteken bijna elke bosbrand die huizen bedreigt
Mensen ontsteken bijna elke bosbrand die huizen bedreigt Diorama-projecten op berenhabitats voor kinderen
Diorama-projecten op berenhabitats voor kinderen Het verschil tussen woestijnplanten en regenwoudplanten
Het verschil tussen woestijnplanten en regenwoudplanten  Nieuwe inzichten in hotspots voor biodiversiteit kunnen hen helpen beschermen tegen mogelijke diepzeemijnbouw
Nieuwe inzichten in hotspots voor biodiversiteit kunnen hen helpen beschermen tegen mogelijke diepzeemijnbouw Positieve gevolgen van overstromingen
Positieve gevolgen van overstromingen
Hoofdlijnen
- Wat zijn de 3 aspecten van de wetenschap?
- Hoe werkt ruw ER met Ribosomes?
- Wetenschappers die boomringen bestuderen, zien aanwijzingen over klimaatverandering
- Waarom lachen mensen als ze gekieteld worden?
- Onderzoekers laten zien hoe probiotica de immuniteit van planten versterken
- Wat is het verschil tussen kieming en bestuiving?
- Waarom restaurants willen dat je eten bestelt op je telefoon
- Waarom liegen mensen over dingen die gemakkelijk weerlegd kunnen worden?
- Welk deel van de cel dat dubbele membraan vormt de grens tussen nucleaire inhoud en cytoplasma?
- Door koper gekatalyseerde enantioselectieve trifluormethylering van benzylische radicalen ontwikkeld

- Gels gemaakt van druppeltjes zijn minder stabiel dan gels gemaakt van vaste deeltjes

- Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen

- Nieuwe technologieën voor de productie van medisch therapeutische eiwitten
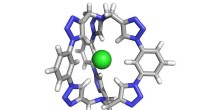
- Een betere zoutvanger bouwen:wetenschappers synthetiseren een moleculaire kooi om chloride op te vangen
 Welke kleur is de kern van de zon?
Welke kleur is de kern van de zon?  NASA's InSight heeft een thermometer voor Mars
NASA's InSight heeft een thermometer voor Mars Moleculaire dynamische simulatie werpt nieuw licht op de vorming van methaanhydraat
Moleculaire dynamische simulatie werpt nieuw licht op de vorming van methaanhydraat Nieuw onderzoek helpt verklaren waarom de zonnewind heter is dan verwacht
Nieuw onderzoek helpt verklaren waarom de zonnewind heter is dan verwacht VS moet de afhankelijkheid van fossiele brandstoffen verminderen, maar partijen zijn het oneens over hoe het moet
VS moet de afhankelijkheid van fossiele brandstoffen verminderen, maar partijen zijn het oneens over hoe het moet Wetenschappers demonstreren microgolfspectrometer die is afgestemd op de Majorana-zoektocht
Wetenschappers demonstreren microgolfspectrometer die is afgestemd op de Majorana-zoektocht Wat is de behoefte van biologische classificatie beantwoord?
Wat is de behoefte van biologische classificatie beantwoord?  Wat zijn nadelen van zonne -energiebron?
Wat zijn nadelen van zonne -energiebron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

