
Wetenschap
Leven niet -metalen waterstofgas van verdunnen. zuren?
Dit is waarom:
* Reactiemechanisme: De bevrijding van waterstofgas van zuren komt meestal voor door een redox -reactie . Een metaalatoom verliest elektronen (oxidatie) en wordt een positief geladen ion, terwijl waterstofionen (H+) van de zuurversterkingselektronen (reductie) om waterstofgas te vormen (H2).
* Niet -metalen en oxidatie: Niet -metalen zijn over het algemeen meer elektronegatief dan waterstof. Dit betekent dat ze een grotere neiging hebben om elektronen te winnen, ze niet te verliezen. Daarom oxideren ze niet gemakkelijk om positieve ionen te vormen.
Voorbeeld:
* metalen: Zink (Zn) reageert met zoutzuur (HCL) om zinkchloride (ZnCl2) en waterstofgas (H2) te produceren:
`` `
Zn (s) + 2HCl (aq) → ZnCl2 (aq) + h2 (g)
`` `
* niet -metalen: Zwavel (S) reageert niet met verdunde zoutzuur. Het blijft niet reactief.
Uitzonderingen:
Er zijn enkele uitzonderingen op deze regel, waarbij sommige niet -metalen kunnen reageren met sterke oxiderende zuren (zoals geconcentreerd salpeterzuur of zwavelzuur). Deze reacties zijn complexer en omvatten mogelijk niet de bevrijding van waterstofgas.
Key Takeaway: Niet -metalen verplaatsen meestal geen waterstof uit verdunde zuren vanwege hun gebrek aan reactiviteit in oxidatieprocessen.
 Methode voor het maken van optisch actieve polymeren met behulp van een spiraalvormig vloeibaar-kristalsjabloon
Methode voor het maken van optisch actieve polymeren met behulp van een spiraalvormig vloeibaar-kristalsjabloon Op zoek naar de chemie van het leven
Op zoek naar de chemie van het leven Scherm kan betere veiligheidstests bieden voor nieuwe chemicaliën
Scherm kan betere veiligheidstests bieden voor nieuwe chemicaliën Grote organische moleculen worden gewoonlijk samengesteld door polymerisatie van een paar soorten waarbij eenvoudige subeenheden worden herhaald. Wat is een uitzondering op deze bewering?
Grote organische moleculen worden gewoonlijk samengesteld door polymerisatie van een paar soorten waarbij eenvoudige subeenheden worden herhaald. Wat is een uitzondering op deze bewering?  Is de ionische verbinding k2so4 oplosbaar in water?
Is de ionische verbinding k2so4 oplosbaar in water?
 Planten die bewegen:hoe Nieuw-Zeelandse soorten zaden verspreiden in een hoogalpiene, natte omgeving
Planten die bewegen:hoe Nieuw-Zeelandse soorten zaden verspreiden in een hoogalpiene, natte omgeving  Hoe sales shopping de planeet doodt
Hoe sales shopping de planeet doodt Wat is een aanpassing van wijnstok?
Wat is een aanpassing van wijnstok?  De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen
De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen Factoren die het weer en klimaat beïnvloeden
Factoren die het weer en klimaat beïnvloeden
Vele factoren beïnvloeden het dagelijkse weer en het klimaat op lange termijn in een bepaalde regio. Gebieden dichter bij de evenaar of op zeeniveau zijn over het algemeen warmer dan gebieden ver van de
Hoofdlijnen
- Chimpanseepopulaties vertonen een grote genetische diversiteit, met gevolgen voor het natuurbehoud
- Wat is een systeem dat bestaat uit de darmen en longen van de nieren leverhuid en longen zuivert het lichaam door afvalmateriaal te elimineren?
- Wat is het eindproduct van mitochondriën?
- De naam gegeven aan een organisme dat de minste verwarring veroorzaakt en hetzelfde is in een taal of land de?
- Welke term beschrijft de verschillen in concentraties van een stof over cellenmembraan?
- Kunnen herten aanwijzingen bevatten over het verband tussen malariaresistentie en sikkelcelziekte?
- Wat eten cecropia -motten?
- Waarom komen wetenschappers op het gebied van wetenschapsgebied?
- Wat is een voorbeeld van interactie tussen het ecosysteem van biotische en abiotische verbindingen?
- Onderzoek peilt naar de moleculaire bouwstenen voor lichtgevoelige materialen

- Snellere ontdekking van medicijnen om onbetrouwbare doelen te bereiken

- Waarom een paar druppels water whisky beter laten smaken

- Nrl ontvangt patent voor koolstofafvangapparaat - een belangrijke stap in de productie van synthetische brandstof uit zeewater
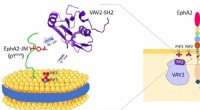
- Wetenschappers onthullen dubbele specificiteit van Vav2-SH2-eiwit
 Een nieuwe benadering voor het bestuderen van elektrische ladingsarrangementen in een supergeleider
Een nieuwe benadering voor het bestuderen van elektrische ladingsarrangementen in een supergeleider Welke plaatgrens is in de Himalaya -bergen?
Welke plaatgrens is in de Himalaya -bergen?  Phonon-hydrodynamica en thermische geleidbaarheid bij ultrahoge kamertemperatuur in dun grafiet
Phonon-hydrodynamica en thermische geleidbaarheid bij ultrahoge kamertemperatuur in dun grafiet Nieuw model kan wetenschappers helpen bij het ontwerpen van materialen voor kunstmatige fotosynthese
Nieuw model kan wetenschappers helpen bij het ontwerpen van materialen voor kunstmatige fotosynthese Wat is bacteriële spore?
Wat is bacteriële spore?  Wanneer de allelen aanwezig zijn voor een eigenschap hetzelfde zijn. genen genaamd?
Wanneer de allelen aanwezig zijn voor een eigenschap hetzelfde zijn. genen genaamd?  Is het waar dat de grotere planeet meer zwaartekracht heeft?
Is het waar dat de grotere planeet meer zwaartekracht heeft?  Noem de 7 belangrijkste tektonische platen die bestanden continenten en de Stille Oceaan?
Noem de 7 belangrijkste tektonische platen die bestanden continenten en de Stille Oceaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

