
Wetenschap
Wat gebeurt er als water verandert van een vaste in vloeibare damp?
1. Smelten (vast tot vloeistof):
* Energie -input: Warmte -energie wordt geabsorbeerd door het ijs, waardoor de moleculen sneller trillen.
* Moleculaire verandering: De bindingen houden de ijsmoleculen in een rigide, kristallijne structuur verzwakken en breken. De moleculen krijgen voldoende energie om vrijer te bewegen, wat resulteert in een vloeibare toestand.
* Temperatuur: De temperatuur blijft tijdens het smeltproces bij 0 ° C (32 ° F), omdat alle energie wordt gebruikt om de bindingen te verbreken.
2. Koken/verdamping (vloeistof tot damp):
* Energie -input: Meer warmte -energie wordt geabsorbeerd door het vloeibare water.
* Moleculaire verandering: Watermoleculen krijgen nog meer kinetische energie en breken los van het oppervlak van de vloeistof. Ze komen de gasvormige fase binnen en vormen waterdamp.
* Temperatuur: De temperatuur blijft bij 100 ° C (212 ° F) tijdens het koken bij standaard atmosferische druk, omdat de energie wordt gebruikt om de krachten te overwinnen die de moleculen in de vloeibare toestand houden. Verdamping kan optreden bij temperaturen onder het koken, maar de snelheid is langzamer.
Sleutelpunten:
* Faseverandering: Deze processen zijn faseveranderingen , waarbij de toestand van materie verandert, maar de chemische samenstelling (H₂o) hetzelfde blijft.
* Energieoverdracht: Zowel smelten als koken vereisen energie -input om de bindingen te verbreken die de moleculen bij elkaar houden.
* omkeerbaarheid: Deze processen zijn omkeerbaar:damp kan tot vloeistof condenseren en vloeistof kan tot vaste stof bevriezen.
Laat het me weten als je meer details over een van deze fasen wilt!
 Snel, nauwkeurig en niet-destructief:de nieuwe methode om voedselkwaliteit te analyseren
Snel, nauwkeurig en niet-destructief:de nieuwe methode om voedselkwaliteit te analyseren Hoeveel magnesiumatomen zouden nodig zijn om te reageren met één broommolecuul?
Hoeveel magnesiumatomen zouden nodig zijn om te reageren met één broommolecuul?  Wat is de formule voor platina II -oxide?
Wat is de formule voor platina II -oxide?  Hoe schrijf je de uitgebalanceerde chemische vergelijking voor de reactie van waterig broomwaterstofzuur reageert met natriumhydroxide om vloeibaar water en bromide te vormen?
Hoe schrijf je de uitgebalanceerde chemische vergelijking voor de reactie van waterig broomwaterstofzuur reageert met natriumhydroxide om vloeibaar water en bromide te vormen?  Om metaal te verfijnen zodat het kan worden bewerkt?
Om metaal te verfijnen zodat het kan worden bewerkt?
Hoofdlijnen
- Plagen van wespen? Een wetenschapper legt uit waarom je niet in paniek moet raken over geruchten over een groeiende bevolking
- Waarom worden reuzenpanda’s zo klein geboren?
- Australische soorten hebben een onafhankelijke kampioen nodig
- Uit welk gen komt alcoholisme?
- Welke term beschrijft de theorie dat leven voortkomt uit leven?
- De VS bevorderen de herziening van de lithiummijn in Nevada vanwege zorgen over bedreigde wilde bloemen
- Waar is Beagle 2? De zoektocht gaat door
- Sprinten richting uitsterven? Het aantal cheetahs daalt wereldwijd
- Hoe wordt een goed opgeleide gok genoemd in de wetenschap?
- Nieuw biosensor-zymonzuur toont veranderingen in pH-waarde

- Unieke interface en onverwacht gedrag helpen verklaren hoe zware metalen werken
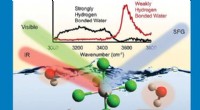
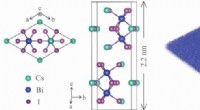
- De kansen zijn goed voor een unieke 2D-compound
- Glycerolfosfaat dient als een terminator van glycaanverlenging bij kanker maligniteiten

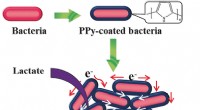
- Geleidende schaal voor bacteriën
 Wat is de geaccepteerde waarde voor NH4CL van oplossingen?
Wat is de geaccepteerde waarde voor NH4CL van oplossingen?  Wat zijn enkele kenmerken van Joviaanse planeten?
Wat zijn enkele kenmerken van Joviaanse planeten?  Wat is één manier waarop en welk ecosysteem een cultuur kan beïnvloeden?
Wat is één manier waarop en welk ecosysteem een cultuur kan beïnvloeden?  Zelfontbranding in nanobellen
Zelfontbranding in nanobellen Hoe veranderde de snelheid van uw golf met variërende amplitude?
Hoe veranderde de snelheid van uw golf met variërende amplitude?  Kleine maar krachtige precipitaten taaien een structurele legering
Kleine maar krachtige precipitaten taaien een structurele legering Hoe klein is 0,0000003 psi?
Hoe klein is 0,0000003 psi?  Is perchloorzuur een ionische verbinding?
Is perchloorzuur een ionische verbinding?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

