
Wetenschap
Wordt de atoommassa gebruikt voor een element met isotopen?
* isotopen: Isotopen van een element hebben hetzelfde aantal protonen (en dus hetzelfde atoomnummer) maar verschillende aantallen neutronen. Dit betekent dat ze verschillende atoommassa's hebben.
* overvloed: Isotopen komen in de natuur voor met verschillende overvloed. Carbon-12 (6 protonen, 6 neutronen) is bijvoorbeeld de meest voorkomende isotoop van koolstof, terwijl koolstof-13 (6 protonen, 7 neutronen) en koolstof-14 (6 protonen, 8 neutronen) minder overvloedig zijn.
* Gemiddelde atoommassa: De gemiddelde atoommassa wordt berekend door rekening te houden met de massa van alle isotopen van een element en hun relatieve overvloed. Dit gewogen gemiddelde vertegenwoordigt de typische atoommassa van het in de natuur gevonden element.
Voorbeeld:
* Carbon-12 heeft een atomaire massa van 12.0000 AMU en is 98,9% overvloedig.
* Carbon-13 heeft een atoommassa van 13.0034 AMU en is 1,1% overvloedig.
* Carbon-14 is een trace-isotoop en heeft een veel lagere overvloed.
De gemiddelde atoommassa van koolstof wordt berekend als:
(0.989 * 12.0000 AMU) + (0.011 * 13.0034 AMU) + (zeer kleine bijdrage van C-14) ≈ 12.011 Amu
Dus de atoommassa van koolstof op het periodiek systeem is 12.011 AMU, wat de gemiddelde atoommassa van al zijn natuurlijk voorkomende isotopen weerspiegelt.
 Hoe gebruik je het wetenschappelijke woord atoom in een zin?
Hoe gebruik je het wetenschappelijke woord atoom in een zin?  Bevindingen bieden recept voor fijnafstemming van legeringen voor gebruik bij hoge temperaturen
Bevindingen bieden recept voor fijnafstemming van legeringen voor gebruik bij hoge temperaturen Efficiënter omgaan met grondstoffen met behulp van moleculaire transportbanden
Efficiënter omgaan met grondstoffen met behulp van moleculaire transportbanden Nieuw groen oplosmiddel kan onze lucht helpen zuiveren
Nieuw groen oplosmiddel kan onze lucht helpen zuiveren Leg het verschil uit tussen oplosbaarheidsgedrag van glycerol en triglyceriden?
Leg het verschil uit tussen oplosbaarheidsgedrag van glycerol en triglyceriden?
 Studie onthult verontrustende multidrug antibioticaresistentie in afgelegen Arctische bodemmicroben
Studie onthult verontrustende multidrug antibioticaresistentie in afgelegen Arctische bodemmicroben Wat is een bomcycloon? Een atmosferische wetenschapper legt uit
Wat is een bomcycloon? Een atmosferische wetenschapper legt uit Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300
Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300 Wat is een voorbeeld van slib?
Wat is een voorbeeld van slib?  Een nieuwe thermometer om ons klimaat in het verleden te bestuderen
Een nieuwe thermometer om ons klimaat in het verleden te bestuderen
Hoofdlijnen
- 3D-simulatie laat zien hoe de vorm van complexe organen evolueert door natuurlijke selectie
- Wat is de wetenschappelijke naam voor eiken bladhydrangea?
- Wat is het voordeel van het gebruik van wetenschappelijke namen in plaats daarvan gebruikelijk zoals kat of hond?
- Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming
- Onderzoek toont aan hoe neuronen hun eindbestemming bereiken
- Entomoloog ontdekt ongewervelde dieren die in meer kleurencombinaties voorkomen dan alle andere
- Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden
- Wat is de term voor conditie waarin hybride nakomelingen een fenotype vertonen dat halverwege tussen ongelijksoortige eigenschappen van ouderorganismen?
- Wat is een synoniemen voor het wetenschapswoord meniscus?
- Nieuwe technieken om de houdbaarheid van ons voedsel te verbeteren, kunnen het oogstverlies helpen minimaliseren

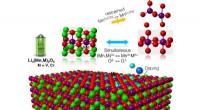
- Onderzoekers voorspellen materialen om lithium-ionbatterijen met recordhoge capaciteit te stabiliseren
- Interdisciplinaire interacties inspireren nieuwe ontdekkingen

- Een 70-jarige benadering van het voorspellen van de microstructuur van materialen weerleggen

- Een nieuwe methode voor kwantitatieve schatting van de mate van overeenkomst van coördinatieveelvlakken

 Hoe Moonshine werkt
Hoe Moonshine werkt  Wat is de nucleaire envelop vergeleken met in een fabriek?
Wat is de nucleaire envelop vergeleken met in een fabriek?  Hoe te bepalen of koper echt is
Hoe te bepalen of koper echt is  Wat is de functie van Cilia in de buurt van de mond?
Wat is de functie van Cilia in de buurt van de mond?  Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?
Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?  Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren
Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren Facebook schrapt 1,5 miljoen video's van Christchurch-aanval, maar kritiek gaat viraal
Facebook schrapt 1,5 miljoen video's van Christchurch-aanval, maar kritiek gaat viraal Hoe klimaatverandering enkele van de iconische vogelsoorten van West-Afrika kan beïnvloeden
Hoe klimaatverandering enkele van de iconische vogelsoorten van West-Afrika kan beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

