
Wetenschap
Welke energie is nodig om twee valentie -elektronen van een metalen atoom te verwijderen?
Dit is waarom:
* ionisatie -energie is de minimale energie die nodig is om een elektron uit een gasvormige atoom of ion in de elektronische toestand van de grond te verwijderen.
* Eerste ionisatie -energie Verwijst naar het verwijderen van het eerste elektron.
* Tweede ionisatie -energie Verwijst naar het verwijderen van het tweede elektron nadat de eerste al is verwijderd.
Factoren die de tweede ionisatie -energie beïnvloeden:
* Nucleaire lading: Een hogere nucleaire lading (meer protonen) trekt elektronen sterker aan, waardoor het moeilijker is om een ander elektron te verwijderen, waardoor de ionisatie -energie wordt vergroot.
* Elektronafscherming: Elektronen in binnenschalen schild buitenste elektronen van de volledige nucleaire lading. Dit afschermingseffect is zwakker bij het verwijderen van het tweede elektron, omdat er één minder elektron is die de kern afschermt.
* Elektronenconfiguratie: Het verwijderen van een elektron uit een gevulde of halfgevulde subschaal vereist meer energie dan het verwijderen van een uit een gedeeltelijk gevulde subshell.
Opmerking: De tweede ionisatie -energie is altijd hoger dan de eerste ionisatie -energie. Dit komt omdat het verwijderen van een elektron uit een positief geladen ion meer energie vereist dan het verwijderen van een uit een neutraal atoom.
Voorbeeld:
De tweede ionisatie -energie van natrium (NA) is bijvoorbeeld 4562 kJ/mol. Dit betekent dat 4562 kJ energie nodig is om het tweede elektron uit een natriumion (Na+) te verwijderen, dat al zijn eerste elektron heeft verloren.
Om de totale energie te berekenen die nodig is om twee valentie -elektronen te verwijderen, zou u de eerste en tweede ionisatie -energieën toevoegen.
 Welke van de volgende verbindingen bevat lood(II)-ionen?
Welke van de volgende verbindingen bevat lood(II)-ionen?  Wanneer natriumcarbonaatoplossing wordt toegevoegd aan Benzocaine Wat is het gas dat evolueert?
Wanneer natriumcarbonaatoplossing wordt toegevoegd aan Benzocaine Wat is het gas dat evolueert?  Waarom koffie gerelateerd aan chemie?
Waarom koffie gerelateerd aan chemie?  Unieke moleculaire CODE:paramagnetische codering van moleculen
Unieke moleculaire CODE:paramagnetische codering van moleculen Wat zijn twee kenmerken van een ideaal gas dat geen echt gas waar is?
Wat zijn twee kenmerken van een ideaal gas dat geen echt gas waar is?
 Beslissingen over watergebruik moeten de veranderende trends in het lokale hydroklimaat weerspiegelen
Beslissingen over watergebruik moeten de veranderende trends in het lokale hydroklimaat weerspiegelen Australië begint op lange termijn naar herstel als het water zich terugtrekt
Australië begint op lange termijn naar herstel als het water zich terugtrekt Afvoer maakt water aan de voet van Niagara Falls zwart
Afvoer maakt water aan de voet van Niagara Falls zwart Studenten demonstreren validiteit van modellen die gebruik maken van gratis, publiek toegankelijke klimaatgegevens
Studenten demonstreren validiteit van modellen die gebruik maken van gratis, publiek toegankelijke klimaatgegevens Wie is de eerste persoon die het bestaan van kleur in licht ontdekt?
Wie is de eerste persoon die het bestaan van kleur in licht ontdekt?
Hoofdlijnen
- Wat verplaatst zuurstof en voedingsstoffen naar de cellen?
- Welke zoogdieren overwinteren?
- Als het diploïde aantal in een levercel 52 is, hoeveel chromosomen zijn er een ei van dit organisme?
- Klaar met de verkiezingen? De wetenschap legt uit hoe de politiek zo verschrikkelijk is geworden
- Welke epitheliale weefsels vormt de opperhuid van de huid?
- Welke wetenschapstak die zich bezighoudt met lesgeven of leraar zijn?
- Testen hoe goed chemische cellen werken, zou een antwoord kunnen bieden op het herkennen van leven
- Wie zijn de wetenschappers die hebben bijgedragen aan de celtheorie en spontane generatie?
- Wat is het grootste lichaamssysteem?
- Een materiaalgeheugen gebruiken om unieke fysieke eigenschappen te coderen
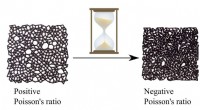
- Ingenieurs 3D-print vormveranderende slimme gel

- Wetenschappers ontdekken hoe malariaparasieten suiker importeren
- Anionen en oplosmiddelen sturen kiemvorming en groei van de vaste elektrolyt-interfase
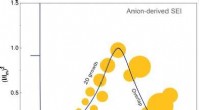
- Een grote stap voorwaarts in organische elektronica

 Cellen geproduceerd aan het einde van Telophase II hebben zoveel chromosomencellen die het proces zijn begonnen.
Cellen geproduceerd aan het einde van Telophase II hebben zoveel chromosomencellen die het proces zijn begonnen.  Welk instrument meet het volume van een blok?
Welk instrument meet het volume van een blok?  Een element met twintig protonen en elektronen krijgt één elektron. In welk type orbitaal past dit?
Een element met twintig protonen en elektronen krijgt één elektron. In welk type orbitaal past dit?  Onderzoekers bieden nieuwe methode om onderzoek naar schone energie te stimuleren
Onderzoekers bieden nieuwe methode om onderzoek naar schone energie te stimuleren Kwelders op de proef gesteld in golfgoot
Kwelders op de proef gesteld in golfgoot  Superhydriden benaderen supergeleiding bij kamertemperatuur bij hoge druk
Superhydriden benaderen supergeleiding bij kamertemperatuur bij hoge druk Uit onderzoek blijkt hoe weinig we weten over vrouwelijke terroristen
Uit onderzoek blijkt hoe weinig we weten over vrouwelijke terroristen  Waarom is energie nodig om te rillen?
Waarom is energie nodig om te rillen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

