
Wetenschap
Hoe verandert overtollige koolstofdioxide de zure basisconditie van een oplossing?
1. CO2 lost op in water: Wanneer CO2 oplost in water, vormt het koolzuur (H2CO3):
CO2 (G) + H2O (L) ⇌ H2CO3 (AQ)
2. Karbonzuur dissocieert: Koolzuurzuur is een zwak zuur dat gedeeltelijk dissocieert in water, waardoor waterstofionen (H+) worden vrijgeeft:
H2CO3 (aq) ⇌ H + (aq) + hco3- (aq)
3. Verhoogde waterstofionen: De afgifte van H+ -ionen verhoogt de concentratie van waterstofionen in de oplossing.
4. Lagere pH: De pH van een oplossing is een maat voor de zuurgraad. Een hogere concentratie van H+ -ionen resulteert in een lagere pH, hetgeen duidt op een meer zure oplossing.
gevolgen van overtollige CO2 in biologische systemen:
* Accoodheid: In het menselijk lichaam leidt overtollige CO2 in het bloed tot een aandoening genaamd ademhalingszuur . Dit kan verschillende symptomen veroorzaken, zoals hoofdpijn, duizeligheid en kortademigheid.
* verzuring van de oceaan: De oceanen absorberen een aanzienlijke hoeveelheid CO2 uit de atmosfeer. Dit leidt tot verzuring van de oceaan, die het leven in zee kan schaden, met name organismen met calciumcarbonaatschalen.
Samenvattend: Overmaat kooldioxide in een oplossing verhoogt de concentratie van waterstofionen, waardoor de oplossing zuurder wordt. Dit heeft belangrijke gevolgen voor biologische systemen, waaronder het menselijk lichaam en de oceanen.
 5 dingen die u moet weten over het nieuwe VN-rapport over klimaatverandering
5 dingen die u moet weten over het nieuwe VN-rapport over klimaatverandering Meerfasige buffering door ammoniak verklaart een breed scala van atmosferische aërosolzuurgraad
Meerfasige buffering door ammoniak verklaart een breed scala van atmosferische aërosolzuurgraad Europa met dezelfde door lockdown veroorzaakte daling van de vervuiling als waargenomen in China
Europa met dezelfde door lockdown veroorzaakte daling van de vervuiling als waargenomen in China Belangrijke landvormen in de VS.
Belangrijke landvormen in de VS.  Door droogte getroffen tondeldoos Californië zet zich schrap voor branden in de komende maanden
Door droogte getroffen tondeldoos Californië zet zich schrap voor branden in de komende maanden
Hoofdlijnen
- Welke cellen van het lichaam zijn het meest gevoelig voor stralingsschade?
- Wat is de functie van een transportsysteem in het levende organisme?
- Begrijpen hoe cellen obstakels vermijden tijdens het navigeren door complexe omgevingen
- Een weefsel dat bestaat uit langgestreepte cellen met meerdere kernen is?
- Behoud oproep aan zaagviskwekerij
- Waarom worden we ziek?
- Wat zijn tests voor eiwitten?
- Welke bio -moleculen zitten in een ribosomen?
- Wetenschappers ontdekken hoe planten grote wortelziekten bestrijden
- Asymmetrische synthese van aziridine met een nieuwe katalysator kan helpen bij de ontwikkeling van nieuwe medicijnen
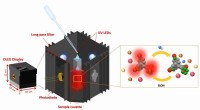
- Nieuw apparaat vereenvoudigt meting van fluorideverontreiniging in water
- Multifunctionele droom keramische matrixcomposieten zijn geboren

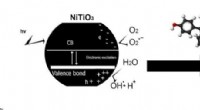
- Chemici zetten titanium nanodeeltjes om in een efficiënt wapen tegen vervuiling
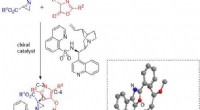
- Wetenschappers stellen nieuwe selectieve reductieve aminekatalysatoren voor met verbeterde stabiliteit

 Wetenschappers ontdekken hoe malariaparasieten suiker importeren
Wetenschappers ontdekken hoe malariaparasieten suiker importeren Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen
Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen Nieuwe visualisatie van zwarte gaten brengt kijkers voorbij de rand
Nieuwe visualisatie van zwarte gaten brengt kijkers voorbij de rand  Onderzoekers bereiken ultrahoge Q-vrije ruimtekoppeling met microtoroid-resonatoren
Onderzoekers bereiken ultrahoge Q-vrije ruimtekoppeling met microtoroid-resonatoren  Waarom overleeft een plant die onder water leeft in het bos?
Waarom overleeft een plant die onder water leeft in het bos?  Welke drie celstructuren die nodig zijn voor fotosynthese?
Welke drie celstructuren die nodig zijn voor fotosynthese?  Hoe marketingactivaverantwoordelijkheid de volledige waarde kan ontsluiten door de activa te meten en te rapporteren
Hoe marketingactivaverantwoordelijkheid de volledige waarde kan ontsluiten door de activa te meten en te rapporteren  Nieuw onderzoek laat zien hoe geclusterde deeltjes de elasticiteit van sommige gels bepalen
Nieuw onderzoek laat zien hoe geclusterde deeltjes de elasticiteit van sommige gels bepalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

