
Wetenschap
Hoeveel bindingen kan koolstof ontstaan bij zichzelf?
Dit is waarom:
* valentie -elektronen: Koolstof heeft vier valentie -elektronen, wat betekent dat het vier bindingen kan vormen.
* Sterke bindingen: De bindingskoolstof vormt zich bij zichzelf (C-C-bindingen) zijn erg sterk.
* variëteit van binding: Koolstof kan enkele, dubbele en drievoudige bindingen vormen met zichzelf.
Dit vermogen om lange ketens en complexe structuren te vormen, is de basis voor de enorme diversiteit van organische moleculen, waaronder:
* koolwaterstoffen: Ketens en ringen van koolstofatomen die aan waterstof zijn gebonden.
* polymeren: Lange ketens van herhalende eenheden.
* eiwitten: Complexe moleculen bestaande uit aminozuren die aan elkaar zijn gekoppeld.
* DNA en RNA: Genetisch materiaal dat een complexe structuur van gekoppelde koolstofatomen bevat.
Dus, hoewel koolstof vier bindingen met andere atomen kan vormen, creëert het vermogen om zich eindeloos te binden met zichzelf een bijna oneindig aantal mogelijkheden.
 Een nieuw type metallacroonether op basis van polyoxometalaat opent onderzoeksmogelijkheden
Een nieuw type metallacroonether op basis van polyoxometalaat opent onderzoeksmogelijkheden  Nieuwe technologie voor detectie van pathogenen aangedreven door lasers
Nieuwe technologie voor detectie van pathogenen aangedreven door lasers Platform optimaliseert het ontwerp van nieuwe, afstembare katalytische systemen
Platform optimaliseert het ontwerp van nieuwe, afstembare katalytische systemen Hoe verhoudt opgeslagen chemische energie zich tot bindingen?
Hoe verhoudt opgeslagen chemische energie zich tot bindingen?  Worden atomen veranderd in chemische reacties volgens de atomaire theorie?
Worden atomen veranderd in chemische reacties volgens de atomaire theorie?
Hoofdlijnen
- Wat voor soort plant is een chickweed?
- Voorbeelden van organismen waarvan de cellen kernen bevatten?
- Droogte geen dingo's achter het uitsterven van tijgers op het vasteland van Australië:studie
- Waarom lopen mensen meestal in dezelfde richting?
- Een nefon bestaat uit een niercorpuscle en wat?
- Wat is het nut van chloroform in DNA -extractie uit organismen?
- Alles wat je nooit wilde weten over bedwantsen, en meer
- Waar vindt de transcriptie van ribonucleïnezuur RNA plaats in een cel?
- Wat zijn oplosbare eiwitten?
- Vooruitgang in de richting van het aansluiten van een antibioticapomp

- Het beoordelen van de risico's van vetwerende chemicaliën in voedselverpakkingen vereist nieuwe methoden, studies

- Less is more:een zachte, zelfaangedreven pomp om mechatronische apparaten te vereenvoudigen
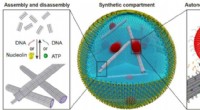
- Nog een stap in de richting van synthetische cellen
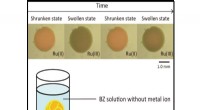
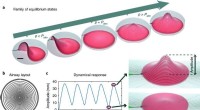
- Door pneumatiek te combineren met een hydrogel om een baromorf te creëren - voor zachte robotica
 Voordelen elektronenmicroscoop
Voordelen elektronenmicroscoop  Minder bevooroordeelde gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp
Minder bevooroordeelde gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp  Extreme telescopen vinden de op één na snelst draaiende pulsar
Extreme telescopen vinden de op één na snelst draaiende pulsar Waar zijn de jongste rotsen in de verspreiding van zeebodem?
Waar zijn de jongste rotsen in de verspreiding van zeebodem?  Wat is de moleculaire formule voor Eicosane met 20 koolstofatomen?
Wat is de moleculaire formule voor Eicosane met 20 koolstofatomen?  Is het vinden van reptielenfossielen vreemd of onverwacht in Antarctica?
Is het vinden van reptielenfossielen vreemd of onverwacht in Antarctica?  Astronomen meten de massa van de Melkweg door te berekenen hoe moeilijk het is om te ontsnappen
Astronomen meten de massa van de Melkweg door te berekenen hoe moeilijk het is om te ontsnappen  Piramide pakt gezondheids- en klimaateffecten van voedsel aan
Piramide pakt gezondheids- en klimaateffecten van voedsel aan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

