
Wetenschap
Wat voor soort basis en zuur is kooldioxide zwak of sterk?
Dit is waarom:
* zwak zuur: Wanneer Co₂ oplost in water, reageert het op koolstofzuur (H₂co₃):
Co₂ (G) + H₂o (L) ⇌ H₂co₃ (aq)
* koolzuur is een zwak zuur: Het ioniseert slechts gedeeltelijk in water, wat betekent dat het niet al zijn waterstofionen (H⁺) aan de oplossing doneert. Dit resulteert in een relatief lage concentratie van H⁺ -ionen, waardoor de oplossing zwak zuur wordt.
* evenwicht: De reactie tussen CO₂ en water is een evenwichtsreactie. Dit betekent dat de vorming van koolzuur omkeerbaar is en dat een deel van het koolzuur terugbreekt in co₂ en water.
Belangrijke opmerking: Hoewel Co₂ fungeert als een zwak zuur in water, is het geen basis. Het heeft niet de mogelijkheid om protonen (H⁺) te accepteren zoals een basis zou doen.
 Is waterstof een element of een samengesteld homogeen mengsel, heterogeen mengsel?
Is waterstof een element of een samengesteld homogeen mengsel, heterogeen mengsel?  Wat zijn de wetenschappelijke principes achter gitaar?
Wat zijn de wetenschappelijke principes achter gitaar?  Welke verbinding ontstaat wanneer salpeterzuur wordt geneutraliseerd?
Welke verbinding ontstaat wanneer salpeterzuur wordt geneutraliseerd?  VS worstelt om bij te blijven terwijl de hennepindustrie groeit
VS worstelt om bij te blijven terwijl de hennepindustrie groeit Osmose-experimenten met aardappelen voor kinderen
Osmose-experimenten met aardappelen voor kinderen
Hoofdlijnen
- Wat is een logische verklaring die in de wetenschap wordt genoemd?
- Wat is bacteriën een omnivoor?
- Waarom worden bananen gebruikt bij DNA -extractie?
- Is het Amerikaanse immigratiebeleid 'STEMming'-innovatie?
- Onderzoek laat zien hoe landbouwgronden de verspreiding van bijenziekten beïnvloeden
- Wat zijn verschillende functies van wortels in planten?
- Hoe cheeta's leeuwen en hyena's te slim af zijn
- Welke organel functioneert in de opslag als water en biomoleculen?
- Hoe cellen hun eigen vloeibare componenten 'opeten'
- Actieve kool kan leiden tot geurloze luiers

- Video:doet melatonine iets?

- On-the-fly analyse van hoe katalysatoren veranderen tijdens reacties om de prestaties te verbeteren

- Zijde kan de gevoeligheid verbeteren, flexibiliteit van draagbare lichaamssensoren

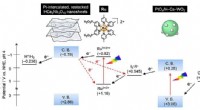
- Nieuwe fotokatalysator verhoogt de efficiëntie van watersplitsing voor schone waterstofproductie
 Waar wordt zwavel gewonnen?
Waar wordt zwavel gewonnen?  Goedkoop blik pakt een grote klap uit voor de toekomst van supercondensatoren
Goedkoop blik pakt een grote klap uit voor de toekomst van supercondensatoren Hoe wist een planeet zijn baan?
Hoe wist een planeet zijn baan?  Bordeaux hoopt op verwoeste wijngaarden in junibloei
Bordeaux hoopt op verwoeste wijngaarden in junibloei De huid of verbergen van een dier begint met P?
De huid of verbergen van een dier begint met P?  Natuurlijke selectie is iets beschreven als overleving van de sterkste, wat meet het meest nauwkeurig een fitheid van het organisme?
Natuurlijke selectie is iets beschreven als overleving van de sterkste, wat meet het meest nauwkeurig een fitheid van het organisme?  Is vocht een mengselverbinding of oplossing?
Is vocht een mengselverbinding of oplossing?  Hoeveel koolstofatomen bevat Butyl?
Hoeveel koolstofatomen bevat Butyl?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

