
Wetenschap
Wat is ontbinding en herkristallisatie?
Oplossing en herkristallisatie:een zuiveringskracht
Oplossing en herkristallisatie zijn twee fundamentele processen in de chemie die vaak samen worden gebruikt voor het zuiveren van vaste verbindingen. Ze maken gebruik van de oplosbaarheidsverschillen van een verbinding in verschillende oplosmiddelen bij verschillende temperaturen.
1. Oplossing:
* Dit is het proces van het oplossen van een vaste verbinding in een vloeibaar oplosmiddel.
* De keuze van het oplosmiddel is cruciaal en hangt af van de oplosbaarheidseigenschappen van de verbinding.
* Ideale oplosmiddelen Voor ontbinding zijn die die:
* Los de gewenste verbinding gemakkelijk op bij hoge temperaturen (meestal kookpunt).
* Los onzuiverheden minimaal op bij alle temperaturen.
* worden gemakkelijk verdampt Om de gezuiverde verbinding te herstellen.
2. Herkristallisatie:
* Dit proces omvat het kristalliseren van de gewenste verbinding uit de oplossing door de omstandigheden te veranderen om de neerslag ervan te bevorderen.
* Meestal omvat dit het koelen van de oplossing Na oplossing neemt de oplosbaarheid van de meeste verbindingen af met lagere temperaturen.
* Deze verandering in oplosbaarheid zorgt ervoor dat de opgeloste verbinding uit de oplossing komt In een zeer pure kristallijne vorm, waardoor onzuiverheden achterblijven in de oplossing.
Hoe ze samenwerken voor zuivering:
* Stap 1:ontbinding :De onzuivere verbinding wordt opgelost in een heet oplosmiddel, waardoor de gewenste verbinding oplost, maar onzuiverheden blijven niet opgelost.
* Stap 2:Filtratie :De hete oplossing wordt gefilterd om onopgeloste onzuiverheden te verwijderen.
* Stap 3:herkristallisatie :De oplossing wordt langzaam afgekoeld, waardoor de gewenste verbinding wordt uitgekristalliseerd naarmate de oplosbaarheid afneemt.
* Stap 4:Filtratie :De kristallen worden gescheiden van de oplossing door filtratie, waardoor onzuiverheden in de resterende oplossing achterblijven.
* Stap 5:wassen :De kristallen worden gewassen met koud oplosmiddel om eventuele resterende onzuiverheden die zich aan hun oppervlak houden te verwijderen.
* Stap 6:Drogen :De kristallen worden gedroogd om elk restoplosmiddel te verwijderen.
Belangrijkste voordelen van herkristallisatie:
* Hoge zuiverheid :Verwijdert onzuiverheden door hun oplosbaarheidsverschillen te benutten.
* Verbeterde kristalmorfologie :Produceert grote, goed gedefinieerde kristallen, waardoor hun eigenschappen worden verbeterd.
* Geschikt voor grootschalige productie :Kan worden opgeschaald voor industriële toepassingen.
Voorbeelden van herkristallisatie:
* zuivering van suiker :Suiker oplost in heet water en het vervolgens afkoelen om de zuivere suiker te kristalliseren.
* Bereiding van farmaceutische geneesmiddelen :Uitgebreid worden gebruikt om actieve ingrediënten in de geneeskunde te zuiveren.
* Synthese van organische verbindingen :Een cruciale stap in de synthese van veel organische verbindingen om pure producten te verkrijgen.
Over het algemeen zijn ontbinding en herkristallisatie krachtige technieken die aanzienlijk bijdragen aan de zuivering van vaste verbindingen en een cruciale rol spelen in verschillende wetenschappelijke en industriële toepassingen.
 Record droogte grijpt Duitse graanschuur in de greep
Record droogte grijpt Duitse graanschuur in de greep Hoe het milieu is veranderd sinds de eerste aardedag 51 jaar geleden
Hoe het milieu is veranderd sinds de eerste aardedag 51 jaar geleden  Wat is de Verzengende Zone?
Wat is de Verzengende Zone?
De verzengende zone verwijst naar het gebied van de aarde nabij de evenaar. Zoals de naam al doet vermoeden, is de verzengende zone over het algemeen warm. Het heeft een nat en droog seizoen, maar ervaart niet de vier se
 Wat beïnvloedt de natuurlijke selectie?
Wat beïnvloedt de natuurlijke selectie?  Nul netto-uitstoot in 2050:een enorme uitdaging voor de luchtvaartindustrie
Nul netto-uitstoot in 2050:een enorme uitdaging voor de luchtvaartindustrie
Hoofdlijnen
- Op AI gebaseerde screeningmethode zou de snelheid van nieuwe geneesmiddelenontdekking kunnen verhogen
- Verschillende Agar-platen
- Wat is een micro-oranisme?
- Sikkelcelanemie is een ziekte die wordt aangenomen door autosomale recessieve erfenis. Wat is de kans dat die persoon die twee ouders heeft, een drager van het defect gen zal zijn?
- Your Brain On: Exam Stress
- Beren hebben geen last van een dieet met veel verzadigde vetten
- Heeft een virus celmembranen?
- Wat voor soort eigenschap is een aanpassing?
- Hoe wordt eiwitten gebruikt door een organisme?
- Autonoom groeiende synthetische DNA-strengen

- Buitengewoon dikke organische light-emitting diodes lossen zeurende problemen op

- Fluorescerende sonde kan kanker verlichten
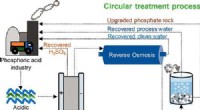
- Wetenschappers ontwikkelen een methode om gevaarlijk zuur industrieel afvalwater om te zetten in waardevolle hulpbronnen
- Onderzoekers rapporteren over live intracellulaire beeldvorming met nieuwe, voorwaardelijk actieve immunofluorescentieprobe
 Studie werpt nieuw licht op visserij door de geschiedenis heen
Studie werpt nieuw licht op visserij door de geschiedenis heen Gegevens tonen aan dat migratie sterker verband houdt met aspiratie dan met wanhoop
Gegevens tonen aan dat migratie sterker verband houdt met aspiratie dan met wanhoop Hoeveel voet en inches in 2,5 m?
Hoeveel voet en inches in 2,5 m?  Moleculaire diepteprofilering gemodelleerd met behulp van buckyballs en energiezuinig argon
Moleculaire diepteprofilering gemodelleerd met behulp van buckyballs en energiezuinig argon Chauffeurs vermijden zware straffen door onder de drempel te blijven
Chauffeurs vermijden zware straffen door onder de drempel te blijven Hoe Mars in de nachtelijke hemel te vinden
Hoe Mars in de nachtelijke hemel te vinden Wat zijn lobben in een kern?
Wat zijn lobben in een kern?  Denken wetenschappers dat een aardbeving West-Californië zou kunnen laten zinken?
Denken wetenschappers dat een aardbeving West-Californië zou kunnen laten zinken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

