
Wetenschap
Hoe bindt natrium- en chloorbinding?
1. Elektronegativiteit: Chloor is veel elektronegatiefer dan natrium. Dit betekent dat chloor een sterkere aantrekkingskracht heeft op elektronen.
2. Elektronenoverdracht: Natrium, met slechts één elektron in zijn buitenste schaal, verliest gemakkelijk dit elektron om een stabiele, gevulde buitenste schaal te bereiken. Chloor, die nog een elektron nodig heeft om zijn buitenste schaal te vullen, accepteert gemakkelijk het elektron van natrium.
3. ionenvorming: Natrium verliest een elektron en wordt een positief geladen ion (Na+). Chloor krijgt een elektron en wordt een negatief geladen ion (Cl-).
4. Elektrostatische aantrekkingskracht: De tegenovergestelde ladingen van de natrium- en chloorionen trekken elkaar sterk aan en vormen een ionische binding.
5. kristalrooster: Veel natrium- en chloorionen rangschikken zichzelf in een regelmatig, herhaaldelijk patroon dat een kristalrooster wordt genoemd, waardoor een vaste, kristallijne structuur ontstaat.
Samenvattend:
* Natrium (NA) en chloor (CL) vormen een ionische binding.
* Natrium verliest een elektron om een positief geladen ion te worden (Na+).
* Chloor krijgt een elektron om een negatief geladen ion te worden (Cl-).
* De tegenovergestelde ladingen van de ionen trekken elkaar aan en vormen de ionische binding.
* De resulterende verbinding is natriumchloride (NaCl).
 Wat is de evenwichtige vergelijking wanneer Silver en Sulphur S8 reageren?
Wat is de evenwichtige vergelijking wanneer Silver en Sulphur S8 reageren?  Leg het verschil uit tussen mechanische en chemische verwering?
Leg het verschil uit tussen mechanische en chemische verwering?  Welke observaties maak je bij het reageren van kaliumhydroxide met natriumcarbonaat?
Welke observaties maak je bij het reageren van kaliumhydroxide met natriumcarbonaat?  Welke structuur helpt bij het reguleren van de testentemperatuur?
Welke structuur helpt bij het reguleren van de testentemperatuur?  Op welke twee manieren verschillen mengsels van verbindingen?
Op welke twee manieren verschillen mengsels van verbindingen?
 Welke zintuigen zijn nuttiger bij het beschrijven van kwalitatieve eigenschappen?
Welke zintuigen zijn nuttiger bij het beschrijven van kwalitatieve eigenschappen?  Staten verliezen enige autoriteit van de Clean Water Act onder de nieuwe EPA-regel
Staten verliezen enige autoriteit van de Clean Water Act onder de nieuwe EPA-regel Hoe je kleding de lucht die je inademt beïnvloedt
Hoe je kleding de lucht die je inademt beïnvloedt Extreem weer kan volgende recessie veroorzaken
Extreem weer kan volgende recessie veroorzaken Waarom we gehaktballen groen moeten maken:nieuw onderzoek onderstreept aanzienlijke milieuvoordelen
Waarom we gehaktballen groen moeten maken:nieuw onderzoek onderstreept aanzienlijke milieuvoordelen
Hoofdlijnen
- Waarom vocale bak? Een recent fenomeen onder popmuzikanten:het laagste register wordt door onderzoekers onderzocht
- Welke organismen hebben het grootste probleem met fotorespiratie?
- Definitie van menselijke biologie
- griezelige vraag bij vogelgriep:hoe dood je miljoenen pluimvee
- Klonten als tijdelijke opslag
- Indonesië's selfiesnagende aap uitgeroepen tot Persoon van het Jaar
- Het Y-chromosoom verdwijnt – dus wat zal er met mannen gebeuren?
- Wat is de aanpassing voor een plantencel?
- Wat is de mate van interne en externe orde in organismen?
- Even kijken hoe ijsvorming voorruiten kan houden, hoogspanningsleidingen ijsvrij

- Levensechte scheikunde gemaakt in laboratoriumonderzoek naar manieren om de oorsprong van het leven te bestuderen
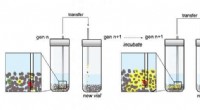
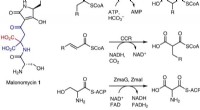
- Wetenschappers ontdekken nieuwe route naar antibiotica met behulp van genbewerking
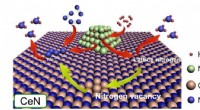
- De leegte in de ammoniaksynthese vullen:de rol van stikstofvacatures in katalysatoren
- Groen waterzuiveringssysteem werkt zonder zware metalen of bijtende chemicaliën

 Macedoniërs zenden SOS uit vanuit het oudste meer van Europa
Macedoniërs zenden SOS uit vanuit het oudste meer van Europa Welke invloed heeft het type materiaal op de weerstand?
Welke invloed heeft het type materiaal op de weerstand?  Wat zijn de 12 subregio's van Texas?
Wat zijn de 12 subregio's van Texas?  Barbie op 60-jarige leeftijd:instrument van vrouwelijke onderdrukking of positieve invloed?
Barbie op 60-jarige leeftijd:instrument van vrouwelijke onderdrukking of positieve invloed?  Onderzoekers lichtcellen op met nanosheets voor kankerbehandeling
Onderzoekers lichtcellen op met nanosheets voor kankerbehandeling Onderzoekers gebruiken machine learning om behandelingen met coronavirus te ontdekken
Onderzoekers gebruiken machine learning om behandelingen met coronavirus te ontdekken Onderzoek toont aan dat de hydrauliek van planten stromend elektrisch potentieel creëert, synchroon met de biologische klok
Onderzoek toont aan dat de hydrauliek van planten stromend elektrisch potentieel creëert, synchroon met de biologische klok  Energie majors geven 90% uit aan fossiele brandstoffen ondanks klimaatbeloften
Energie majors geven 90% uit aan fossiele brandstoffen ondanks klimaatbeloften
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

