
Wetenschap
Welke elementen vormen gewoonlijk covalente bindingen?
Dit is waarom:
* elektronegativiteit: Niet -metalen hebben over het algemeen een hoge elektronegativiteit, wat betekent dat ze een sterke aantrekkingskracht hebben op elektronen. Ze verliezen minder kans om elektronen te verliezen en deelt ze eerder om ze te delen om een stabiele elektronenconfiguratie te bereiken.
* Elektronen delen: Covalente binding omvat het delen van elektronen tussen atomen om een stabiel molecuul te vormen. Niet-metalen zijn goed geschikt voor dit type binding omdat ze een volledige buitenste schaal van elektronen kunnen bereiken door te delen.
Gemeenschappelijke voorbeelden van elementen die covalente bindingen vormen, omvatten:
* Groep 14 (koolstofgroep): Koolstof (C), Silicon (SI), Germanium (GE)
* Groep 15 (stikstofgroep): Stikstof (n), fosfor (p), arseen (as)
* Groep 16 (zuurstofgroep): Zuurstof (O), zwavel (s), selenium (SE)
* Groep 17 (halogenen): Fluor (F), chloor (CL), broom (Br), jodium (i)
Belangrijke opmerking:
Hoewel niet -metalen voornamelijk covalente bindingen vormen, zijn er enkele uitzonderingen. Waterstof (H) is bijvoorbeeld een niet -metaal, maar het kan ook ionische bindingen vormen met zeer elektronegatieve elementen zoals zuurstof (O) om water te vormen (H₂o).
Laat het me weten als je meer details wilt over specifieke covalente bindingstypen of voorbeelden!
 Kan lithium genezen wat de Saltonzee scheelt?
Kan lithium genezen wat de Saltonzee scheelt?  Wat gebeurt er wanneer waterstof en zuurstof combineren?
Wat gebeurt er wanneer waterstof en zuurstof combineren?  Hoeveel mol zijn gelijk aan 5.7510 24 atomen van Al?
Hoeveel mol zijn gelijk aan 5.7510 24 atomen van Al?  Door polyurethaan afbreekbaar te maken, krijgen de componenten een tweede leven
Door polyurethaan afbreekbaar te maken, krijgen de componenten een tweede leven Kunnen alle vloeistoffen worden gemengd om oplossingen te creëren?
Kunnen alle vloeistoffen worden gemengd om oplossingen te creëren?
 Afvaleilanden voor de kust van Midden-Amerika duiden op een probleem met oceaanvervuiling
Afvaleilanden voor de kust van Midden-Amerika duiden op een probleem met oceaanvervuiling Dode zones kunnen wereldwijd koraalriffen bedreigen
Dode zones kunnen wereldwijd koraalriffen bedreigen Wetenschappers werpen nieuw licht op de rol van virussen bij koraalverbleking
Wetenschappers werpen nieuw licht op de rol van virussen bij koraalverbleking Hoe spinnen paren
Hoe spinnen paren  Het Panamakanaal voorkomt voorlopig een crisis, maar ten koste van het drinkwater
Het Panamakanaal voorkomt voorlopig een crisis, maar ten koste van het drinkwater
Hoofdlijnen
- Twee als het over land gaat? Biologen ontdekken dodelijk TTX-toxine in twee terrestrische soorten
- Onderzoek laat zien hoe verschillen in mannelijke en vrouwelijke hersenen ontstaan
- Wat is de definitie van hypothese in de wetenschappelijke methode?
- Hoe kan chromatografie worden gebruikt om aan te tonen dat de hydrolyse van zetmeel slechts één suiker oplevert?
- Wat zijn de eigenschappen van kernen?
- Waar in het lichaam is vitamine D geproduceerd en uit welk molecuul wordt het gewijzigd?
- Drie voorbeelden van een enkelvoudig allel-kenmerk
- Toch niet zo verschillend:menselijke cellen, winterharde microben delen een gemeenschappelijke voorouder
- Nieuw ontdekt eiwit kan worden gebruikt om levensreddende antischimmelmiddelen te produceren
- Hoe microben in starterculturen gefermenteerde worst lekker maken

- Ingenieurs laten zien hoe wolfraamoxide kan worden gebruikt als katalysator in duurzame chemische conversies

- Veelgebruikte medicijnbron voor inzichten in de vorming van vlinderkristallen
- Video:Zou je kunnen slagen voor een drugstest door CBD te nemen?

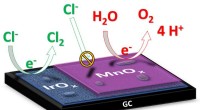
- Een stap dichter bij duurzame energie uit zeewater
 Einstein-brief brengt $ 100 op, 000 op veiling in Jeruzalem
Einstein-brief brengt $ 100 op, 000 op veiling in Jeruzalem Wat is de donkere gekleurde rots die het grootste deel van de oceanische korst vormt?
Wat is de donkere gekleurde rots die het grootste deel van de oceanische korst vormt?  Waarom dachten vroege wetenschappers dat de energiebron van zon was?
Waarom dachten vroege wetenschappers dat de energiebron van zon was?  Peru onthult gigantische kattenets op beroemde Nazca-site
Peru onthult gigantische kattenets op beroemde Nazca-site Schaamte over armoede vergroot vaak armoede
Schaamte over armoede vergroot vaak armoede Large Hadron heeft een geweldige tijd gehad in 2016
Large Hadron heeft een geweldige tijd gehad in 2016  Hoe kun je een levend organisme en machine vergelijken?
Hoe kun je een levend organisme en machine vergelijken?  Zelfaanpassend systeem voor temperatuurregeling:een dynamisch regelbare strategie voor het genezen van wondweefsel
Zelfaanpassend systeem voor temperatuurregeling:een dynamisch regelbare strategie voor het genezen van wondweefsel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

