
Wetenschap
Een stap dichter bij duurzame energie uit zeewater
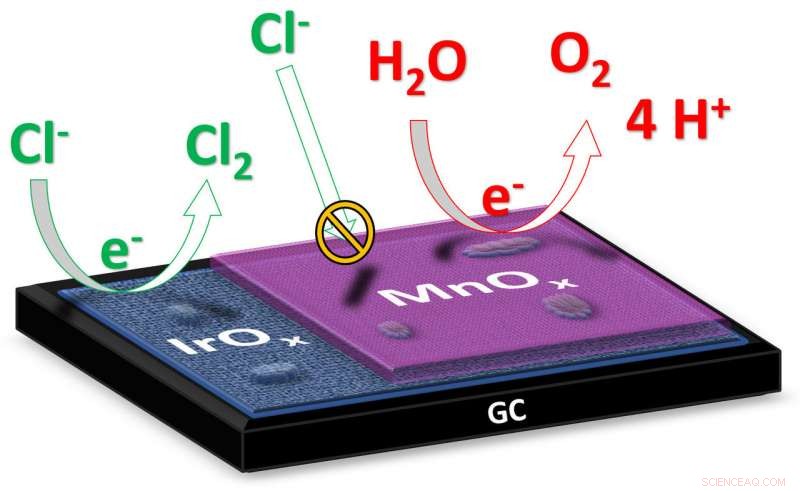
Tijdens de elektrolyse van water, elektriciteit wordt door het water geleid om het in andere stoffen te splitsen. In de gewenste reactie, vloeibaar water (H2O) splitst zich in zuurstofgas (O2) en waterstofgas (H2). Op zout water, natriumchloride (NaCl) is aanwezig als opgeloste natrium- en chloorionen (Na + en Cl - ). In dit geval, een tweede reactie kan ook optreden tijdens de elektrolyse, waarin de chloorionen worden omgezet in chloorgas (Cl 2 ). Credit:Universiteit Leiden
De onderzoeksgroep onder leiding van de Leidse chemicus Marc Koper heeft een katalysator ontdekt die de aanmaak van chloorgas bij zoutwaterelektrolyse minimaliseert. De uitvinding kan de directe productie van waterstof uit zeewater mogelijk maken. Het artikel is gepubliceerd in de Tijdschrift van de American Chemical Society .
"Bij de elektrolyse van zout water, zoals zeewater, het uiteindelijke doel is om waterstof te produceren aan de kathode, " legt promovendus Jan Vos van het Leids Instituut voor Chemie uit. "Het product dat aan de anode wordt gevormd is idealiter zuurstof, want dat is onschadelijk voor het milieu.” bij zoutwaterelektrolyse kan zich ook giftig chloorgas vormen aan de anode. De onderzoekers hebben nu een katalysator geproduceerd die de vorming van chloorgas minimaliseert ten gunste van zuurstofvorming. Vos legt uit:"De katalysator bestaat uit twee metaaloxiden:iridiumoxide met een laag mangaanoxide van slechts een tiental nanometer dik. Iridium is een materiaal dat een hoge katalytische activiteit vertoont voor de vorming van zowel zuurstofgas als chloorgas; het mangaanoxide werkt als een soort membraan dat de toevoer van chloride-ionen verhindert en de vorming van chloorgas onderdrukt."
De elektrolyse van water is een belangrijke stap voor de productie en het gebruik van waterstof als alternatieve energiedrager. Een anode die de vorming van chloorgas tegengaat, maakt waterelektrolyse mogelijk waarbij het niet nodig is eerst het water van opgelost zout te ontdoen, waarvan het proces nog steeds aanzienlijke hoeveelheden energie en kapitaal kost. Het zou de directe productie van waterstof uit zeewater mogelijk maken, waardoor de zeldzame zoetwaterreserves op aarde worden ontlast.
Volgens Vos, een nuttig neveneffect van zoutwaterelektrolyse is de productie van zeer zuiver zoet water. "Als het gewonnen waterstofgas uiteindelijk als brandstof wordt gebruikt, bijvoorbeeld in een brandstofcel van een auto, de waterstof reageert terug tot water met zuurstofgas uit de atmosfeer. Op die manier, de grootschalige toepassing van waterelektrolyse en waterstof in brandstofcellen zal leiden tot grote hoeveelheden van dit 'afvalproduct':zuiver water. In een toekomst waarin watertekorten een steeds nijpender probleem worden, dit zou zeker niet onwenselijk zijn."
Het onderzoek werpt nieuw licht op een vraag in de chemie die al tientallen jaren speelt. "We hadden oorspronkelijk geen idee waarom materialen op basis van mangaanoxide zo'n hoge selectiviteit voor zuurstof hadden. We gingen ervan uit dat het puur een katalytische eigenschap van het materiaal was, maar mogelijke effecten van diffusiebarrières:het selectief blokkeren van het transport van chloride-ionen... Daar dacht ik niet eens aan! In feite, het is een heel basaal, effectieve oplossing voor een zeer complex probleem. Dat heeft onze onderzoeksrichting radicaal veranderd."
De ontdekking heeft gevolgen voor de selectiviteit bij elektrolyse. Selectiviteit is een belangrijk criterium voor hoe goed een katalysator werkt. In veel (elektro-)chemische processen, het is mogelijk om tijdens een reactie verschillende producten te vormen, maar men hoopt dat alleen het vereiste product wordt gevormd. De manier om selectiviteit te beïnvloeden is meestal om de katalysator heel precies te selecteren en te finetunen, maar dit kost veel tijd en geld. Bovendien, het is niet altijd mogelijk om hoge selectiviteit te combineren met hoge activiteit, een ander belangrijk kenmerk.
Volgens Vos, het onderzoek past mooi in een opkomende, alternatieve trend in elektrokatalyse:het gebruik van bepaalde coatings om een katalysator te verbeteren. "Zo'n laag voorkomt dat ongewenste reactanten de katalysator bereiken. Zo kan op een alternatieve manier een actief maar niet-selectief katalytisch materiaal selectief worden gemaakt."
 Surround sound van lichtgewicht roll-to-roll bedrukt luidsprekerpapier
Surround sound van lichtgewicht roll-to-roll bedrukt luidsprekerpapier Techniek maakt afdrukbare en herschrijfbare kleurenafbeeldingen mogelijk
Techniek maakt afdrukbare en herschrijfbare kleurenafbeeldingen mogelijk Bluetooth-apparaat detecteert het fermentatieproces gedurende dagen
Bluetooth-apparaat detecteert het fermentatieproces gedurende dagen Nieuwe techniek maakt de weg vrij voor perfecte perovskieten
Nieuwe techniek maakt de weg vrij voor perfecte perovskieten Verbetering van het vastleggen van koolstof met metaal-organische kaders
Verbetering van het vastleggen van koolstof met metaal-organische kaders
 Aardbevingsangst maakt einde aan Nederlandse gashausse
Aardbevingsangst maakt einde aan Nederlandse gashausse Nieuw onderzoek suggereert minerale nanodeeltjes als alomtegenwoordige enzymnabootsers in aardse systemen
Nieuw onderzoek suggereert minerale nanodeeltjes als alomtegenwoordige enzymnabootsers in aardse systemen Nieuwe tool geeft appelboerderijen hoop in strijd tegen voorjaarsbevriezing
Nieuwe tool geeft appelboerderijen hoop in strijd tegen voorjaarsbevriezing In verschroeiende droogte, Californische boeren verscheuren kostbare amandelbomen
In verschroeiende droogte, Californische boeren verscheuren kostbare amandelbomen Blockadia-kaart onthult wereldwijde schaal van antifossiele brandstofbeweging
Blockadia-kaart onthult wereldwijde schaal van antifossiele brandstofbeweging
Hoofdlijnen
- Hoe zou zout Gist beïnvloeden?
- Theory of Evolution: Definition, Charles Darwin, Evidence & Voorbeelden
- Waarom is UV-licht schadelijk?
- Zijn mannen of vrouwen gelukkiger?
- Antibioticaresistentie: definitie, oorzaken en voorbeelden
- Onderzoek toont een manier om een gemeenschappelijke basis te creëren over gen-editing
- Onderzoeker bestudeert vogels die alle paringsregels overtreden
- Hoe een cellenvorm zijn functie beïnvloedt
- Opnieuw klonen van de eerste gekloonde hond die tot nu toe als succesvol werd beschouwd
- Geblokkeerde beweging in moleculaire motor en rotor

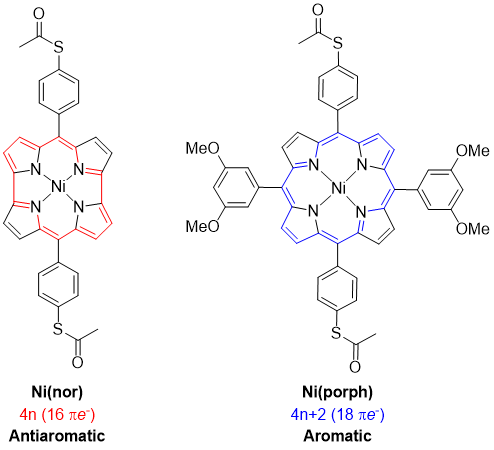
- Anti-aromatisch molecuul vertoont record elektrische geleiding
- Vormverschuivend materiaal kan morphen, keert zichzelf om met behulp van warmte, licht

- Chemicus creëert efficiënte katalysator voor synthese van organische sulfiden

- Betere bètapeptiden bouwen

 Elk bewijs waargenomen met behulp van een kleine anyon-collider
Elk bewijs waargenomen met behulp van een kleine anyon-collider Rek en vloei:onderzoek werpt licht op ongebruikelijke eigenschappen van bekende materialen
Rek en vloei:onderzoek werpt licht op ongebruikelijke eigenschappen van bekende materialen Verschuiving van openbaar vervoer naar privéauto's naarmate COVID-19 zich verspreidt
Verschuiving van openbaar vervoer naar privéauto's naarmate COVID-19 zich verspreidt Natuurkundigen bieden ondersteuning voor retrocausale kwantumtheorie, waarin de toekomst het verleden beïnvloedt
Natuurkundigen bieden ondersteuning voor retrocausale kwantumtheorie, waarin de toekomst het verleden beïnvloedt Drie astronauten vliegen naar het internationale ruimtestation
Drie astronauten vliegen naar het internationale ruimtestation Vaticaan schakelt fonteinen uit terwijl Italië strijdt tegen droogte
Vaticaan schakelt fonteinen uit terwijl Italië strijdt tegen droogte Hoe maak je een 3D-kegelvorm
Hoe maak je een 3D-kegelvorm  Synthese van diamantachtige koolstof nanovezelfilm
Synthese van diamantachtige koolstof nanovezelfilm
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

