
Wetenschap
Waarom voeg je H2SO4 toe aan de KMNO4 -titratie?
1. Om een zure omgeving te bieden:
* kmno₄ is een sterk oxidatiemiddel: Het werkt het beste in zure omstandigheden.
* H₂so₄ biedt het benodigde zuurmedium: Hierdoor kan Kmno₄ gemakkelijker reageren met het reductiemiddel dat wordt getitreerd.
* Optimaliseert de reactie: In zure omstandigheden wordt het MNO₄⁻ -ion gereduceerd tot Mn²⁺, dat kleurloos is. Deze kleurverandering is cruciaal voor eindpuntbepaling in de titratie.
2. Om nevenreacties te voorkomen:
* kmno₄ kan reageren met andere ionen: Het kan bijvoorbeeld reageren met hydroxide -ionen (OH⁻) om MNO₂ (mangaandioxide) te vormen, een bruin neerslag.
* H₂so₄ onderdrukt deze nevenreacties: Het zorgt ervoor dat KMNO₄ voornamelijk reageert met het reductiemiddel dat wordt getitreerd.
3. Om de KMNO₄ -oplossing te stabiliseren:
* Kmno₄ -oplossingen zijn onstabiel in aanwezigheid van licht: Ze kunnen ontleden om Mno₂ te vormen.
* H₂so₄ helpt de oplossing te stabiliseren: Het voorkomt de vorming van MNO₂ door de oplossing zuur te houden.
Samenvattend
Zwavelzuur toevoegen aan een kmno₄ -titratie:
* Biedt een zure omgeving voor de reactie.
* Voorkomt nevenreacties.
* Stabiliseert de KMNO₄ -oplossing.
Dit zorgt voor nauwkeurige en betrouwbare titratieresultaten.
 Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten
Meerdere factoren hebben hun krachten gebundeld om het Great Barrier Reef in 2016 te verwoesten Zware overstromingen treffen centraal China; metro's overstroomd
Zware overstromingen treffen centraal China; metro's overstroomd Wetenschappers ontdekken dat koolstof van ontdooiende permafrost sneller in de atmosfeer wordt vrijgegeven dan eerder werd gedacht
Wetenschappers ontdekken dat koolstof van ontdooiende permafrost sneller in de atmosfeer wordt vrijgegeven dan eerder werd gedacht Het openen van plastic zakken en flessen kan microplastics genereren
Het openen van plastic zakken en flessen kan microplastics genereren Een walviskoor laat zien hoe klimaatverandering de migratie kan veranderen
Een walviskoor laat zien hoe klimaatverandering de migratie kan veranderen
Hoofdlijnen
- Onderzoek werpt nieuw licht op hoe ziekten over verschillende soorten heen springen
- Chimerisme:je kunt je eigen tweeling zijn
- Interne beweging in cellen wordt door wat gebracht?
- Beren hebben geen last van een dieet met veel verzadigde vetten
- Is Rucula een monocot of dicot?
- Microben reizen door de lucht; Het zou goed zijn om te weten hoe en waar
- In eukaryoten worden alleen exons vertaald?
- Hoe helpt genetische combinatie een soort om te overleven?
- Een enzym dat de vorming van het DNA katalyseert Molecuul
- Een supermateriaal dat toepasbaar is op batterijen en andere apparaten voor energieconversie

- Op gallium gebaseerd oplosmiddel analyseert efficiënt optisch actieve alcoholen
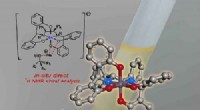
- Groene oplosmiddelen vinden voor gedrukte elektronica

- Efficiëntere scheiding van methaan en CO2
- Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen
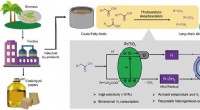
 Typen Bobcats
Typen Bobcats  Waarom zout water en verse mix?
Waarom zout water en verse mix?  Wat is de atomaire structuur van chloor?
Wat is de atomaire structuur van chloor?  Hoeveel meer valentie -elektronen heeft zuurstof nodig om een volledige buitenste te hebben?
Hoeveel meer valentie -elektronen heeft zuurstof nodig om een volledige buitenste te hebben?  Machine learning-technologie om vreemde gebeurtenissen tussen LHC-gegevens te volgen
Machine learning-technologie om vreemde gebeurtenissen tussen LHC-gegevens te volgen Nieuwe uikidama-nanodeeltjesstructuur onthuld
Nieuwe uikidama-nanodeeltjesstructuur onthuld Waarom zoveel middeleeuwse manuscripten doodles bevatten. En wat ze onthullen
Waarom zoveel middeleeuwse manuscripten doodles bevatten. En wat ze onthullen Nieuwe koolstofnanobuisgarens kunnen elektriciteit opwekken uit afvalwarmte
Nieuwe koolstofnanobuisgarens kunnen elektriciteit opwekken uit afvalwarmte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

