
Wetenschap
Hoeveel bindings- en niet-bindende elektronenparen zijn te vinden in de BF3-moleculen?
Hier leest u hoe u het aantal binding en niet-bindende elektronenparen in BF3 kunt bepalen:
1. Lewis -structuur:
* boron (b): Heeft 3 valentie -elektronen.
* fluor (f): Heeft 7 valentie -elektronen.
* Totale valentie -elektronen: 3 (b) + 3 (7) (f) =24
* boron (b): Vormt 3 enkele bindingen met fluor, met behulp van alle 3 van zijn valentie -elektronen.
* fluor (f): Elke fluor vormt een enkele binding met boor, waardoor 6 niet-bindende elektronen (3 eenzame paren) op elk fluoratoom achterblijven.
2. Elektronenparen Count:
* bindparen: 3 (één voor elke B-F-binding)
* Niet-bindende paren: 6 (3 eenzame paren op elk fluoratoom)
Daarom heeft BF3 3 bindingselektronenparen en 6 niet-bindende elektronenparen.
 Stabiliteit van het klimaat op aarde hangt af van Amazonia
Stabiliteit van het klimaat op aarde hangt af van Amazonia Kikkerfossielen vertellen ons iets nieuws over regenpatronen aan de westkust van Zuid-Afrika
Kikkerfossielen vertellen ons iets nieuws over regenpatronen aan de westkust van Zuid-Afrika Wat zijn oriëntatiepunten in het tropische regenwoud?
Wat zijn oriëntatiepunten in het tropische regenwoud?  Waarom overstromingen nog steeds zo moeilijk te voorspellen en voor te bereiden zijn
Waarom overstromingen nog steeds zo moeilijk te voorspellen en voor te bereiden zijn De zorg voor de heuvels beschermt ons tegen overstromingen, zegt nieuw onderzoek
De zorg voor de heuvels beschermt ons tegen overstromingen, zegt nieuw onderzoek
Hoofdlijnen
- Hoe verschilt een plantaardig of dierlijk weefsel van slechts een aggregaat van vergelijkbare cellen?
- Waarom heeft een plant wortels nodig en bladeren?
- Hoe heet het wanneer een bacterie virus gebruikt om zijn DNA een andere bacterie over te dragen?
- Biologen ontdekten meer dan een eeuw geleden wat Przewalski's paard at
- Wat voor soort kenmerken worden gebruikt om vandaag organismen te classificeren?
- Heb je de bacteriële celwand of cytoplasma gekleurd?
- Hoe worden pulsars gevormd?
- Het choroïde en de oorschelp zijn vergelijkbaar omdat?
- Welk sponsachtige weefsel houdt je botten bij elkaar?
- Hergebruik van 1 kg kleding bespaart 25 kg CO2, studie vondsten

- Nieuwe monsterhouder voor eiwitkristallografie

- Nieuw ontworpen liganden voor een katalytische reactie om medicijnen en nuttige verbindingen te synthetiseren

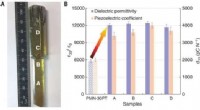
- Onderzoekers ontdekken dat het toevoegen van zeldzame-aarde-elementen aan piëzo-elektrische kristallen de prestaties drastisch verbetert
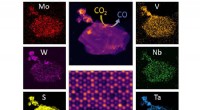
- Nieuwe 2D-legering combineert vijf metalen, breekt koolstofdioxide af
 Een andere kijk op COVID-19
Een andere kijk op COVID-19 Bedreigde Amargosa woelmuizen hebben meer nodig dan een regenachtige dag
Bedreigde Amargosa woelmuizen hebben meer nodig dan een regenachtige dag Papier met een beschrijving van een dinosaurus ter grootte van een kolibrie ingetrokken
Papier met een beschrijving van een dinosaurus ter grootte van een kolibrie ingetrokken Chemische reacties voltooien
Chemische reacties voltooien Covid-19-beperkende inspanningen kunnen de VS op het goede spoor zetten om de doelstellingen van het klimaatakkoord van Parijs te halen
Covid-19-beperkende inspanningen kunnen de VS op het goede spoor zetten om de doelstellingen van het klimaatakkoord van Parijs te halen Een dun gelaagde gesteente samengesteld uit deeltjes ter grootte van klei is een?
Een dun gelaagde gesteente samengesteld uit deeltjes ter grootte van klei is een?  Eigenschappen van Nylon
Eigenschappen van Nylon Hoe ziet een muurwolk eruit?
Hoe ziet een muurwolk eruit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

